Электростатическая адсорбция
Cтраница 2
Поскольку электронная оболочка у сульфат-ионов поляризуется сильнее, чем у хлорид-ионов, электростатическая адсорбция сульфатов проявляется сильнее, чем у хлоридов, и они легче вытесняют с поверхности анионы нитробензойной кислоты. [16]
В работах ряда авторов было детально проанализировано влияние этих эффектов на характер электростатической адсорбции ионов, емкость диффузного двойного слоя и поверхностное натяжение растворов электролитов. В основу этого исследования, как и ранее, был положен метод коррелятивных функций. [17]
Торможение процесса анодного растворения металла при пассивировании в определенной степени может быть вызвано специфической и электростатической адсорбцией ионов, изменяющих величину / - потенциала и образующих поверхностные комплексы, оказывающие определенное влияние на скорость анодного растворения. Однако решающую роль играет изменение строения двойного электрического слоя на поверхности металла и непосредственно на границе металл - раствор. При этом, если происходит образование прочной связи адсорбированного ( хемосорбирован-ного вещества с металлом на всей поверхности, то скорость процесса сильно замедляется. Очевидно, что при пассивировании возможно и неполное покрытие поверхности металла кислородом с образованием поверхностных соединений. В этом случае замедление скорости анодного процесса связано с блокировкой части активной поверхности. [18]
Возникновение избыточного по отношению к заряду металла и объемной концентрации анионов отрицательного заряди на поверхности металла приводит к электростатической адсорбции катионов и изменению знака 1 -потенциала. [19]
Когда же в расплаве присутствует два сорта одноименно заряженных частиц, то в зависимости от соотношения ионных радиусов и концентрации наблюдается преимущественная электростатическая адсорбция в поверхностном слое того или другого вида ионов. [20]
Из соотношения (2.8) следует, что добавление в систему значительных количеств посторонних ионов ( например, многозарядных ионов) должно приводить к уменьшению вторичной электростатической адсорбции радиоактивных изотопов. [21]
В случае четвертичных солей аммония, водород в которых полностью замещен на углеводородные радикалы, можно допустить только один путь воздействия на электродные процессы - электростатическая адсорбция и появление - эффекта. Усиление адсорбции таких производных должно привести к появлению у них высоких ингибиторных свойств. [22]
Индикаторы нейтрализации изменяют окраску в растворе в зависимости от изменения рН среды; окислительно-восстановительные индикаторы - от изменений потенциала раствора; адсорбционные индикаторы - от степени электростатической адсорбции. Флуоресцентные индикаторы изменяют свою окраску при освещении титруемого раствора ультрафиолетовыми лучами и применяются как индикаторы кислотно-щелочные, окислительно-восстановительные и адсорбционные. [23]
Положительная обкладка внутреннего двойного слоя увеличивает положительный заряд поверхности металла и воздействует на структуру двойного электрохимического слоя, оказывая ориентирующее влияние на диполи растворителя и изменяя электростатическую адсорбцию катионов и анионов электролита. [24]
По природе преобладающих сил все типы адсорбции можно разбить на 3 группы: 1) дисперсионную адсорбцию, при которой доминируют лон-доновские дисперсионные силы; 2) электростатическую адсорбцию, при которой преобладают силы взаимодействия между заряженными частицами поверхности и постоянными или наведенными диполями ад сорб-тива, и 3) химическую сорбцию. [25]
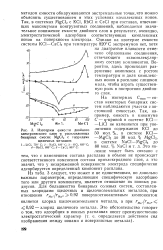 |
Изотермы емко. ти двойного личении содержания КС1 до. [26] |
Так, в системах MgCl2 с КС1, RbCl и CsCl при составах, отвечающих максимумам конгруэнтных соединений, наблюдается значительное понижение емкости двойного слоя в результате, очевидно, электростатической адсорбции соответствующих комплексных ионов на поверхности электрода. [27]
Одну из серьезных трудностей в изучении явлений, обусловленных статистикой элементарных характеристик поверхности, представляет сходство ряда статистических проявлений с явлениями, вызванными взаимным отталкиванием адсорбированных молекул в слое, которое естественно допускать при некоторых типах электростатической адсорбции 3 и которому некоторыми авторами без достаточных оснований приписывается весьма широкое распространение. Из сказанного вытекает целесообразность работы с малыми заполнениями. Для того чтобы при этом чувствительность методики была достаточно велика, целесообразно работать с адсорбентами, отличающимися максимально развитой удельной поверхностью. В то же время желательна высокая устойчивость поверхности к нагреванию. [28]
В случае выделения сплава Cd-Sb хемоеорбционное взаимодействие тартрат-ионов должно ослабевать по сравнению-с сурьмой вследствие меньшей прочности ( комплексов, образующихся с кадмием. Однако электростатическая адсорбция их может усиливаться, поскольку потенциал нулевого заряда кадмия значительно отрицательнее, чем сурьмы, так что поверхность ( сплава при электролизе должна быть заряжена положительно, а не отрицательно, как при осаждении одной сурьмы. В результате усиления электростатической адсорбции тартрат-ионов может возрастать тор ( можение выделения сурьмы на поверхности сплава Cd-Sb по сравнению с чистой сурьмой. Поскольку кадмий присутствует в растворе в виде простых ионов, а не тартратных комплексов, его восстановление ( практически не меняется при изменении адсорбции тартрат-ионов. [29]
Объяснение высоких ингибирующих свойств бромидов алкиларил-фосфониевых солей [148] связано с тем, что эти соединения имеют возможность одновременно адсорбироваться с участием разных адсорбционных центров. Прежде всего, это электростатическая адсорбция катионов фосфония, далее это адсорбция с участием орбиталей я-связи и неспаренных электронов и, наконец, хемосорбция, в которую может переходить второй тип адсорбции и которая завершается химическим превращением исходного иона фосфония. [30]
Страницы: 1 2 3 4