Медленная адсорбция
Cтраница 4
Прежде чем перейти от опытов с никелем к другим вопросам, целесообразно указать на ряд опытов по адсорбции водорода, о которых в разной форме сообщалось в литературе. Выше было доказано, что медленная адсорбция фактически является абсорбцией. [46]
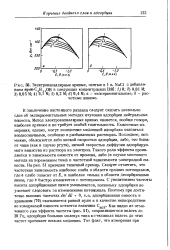
В заключение настоящего раздела следует сказать несколько слов об экспериментальных методах изучения адсорбции нейтральных веществ. Метод электрокапиллярных кривых является, вообще говоря, наиболее прямым и не требует особой тщательности. Емкостные измерения, однако, могут вследствие медленной адсорбции оказаться неоднозначными, особенно в разбавленных растворах. Последнее, возможно, объясняется либо низкой скоростью адсорбции, либо, что бывает чаще ( как в случае ртути), низкой скоростью диффузии адсорбируемого вещества из раствора на электрод. Такого рода эффекты проявляются в зависимости емкости от времени, либо ( в случае мостового метода на переменном токе) в частотной зависимости электродной емкости. На рис. 51 приведен типичный пример. Следует отметить, что частотная зависимость наиболее слаба в области средних потенциалов, где в слабо зависит от Е, и наиболее сильна в области десорбционных пиков, где 9 быстро изменяется с потенциалом. Как видно из отмеченного уже эффекта частоты ( рис. 51), сохраняющегося вплоть до 20 Гц, адсорбция больших молекул типа к-гексанола вплоть до этих частот протекает весьма медленно. [48]
Более интересны работы Дзидзима [7] по изучению адсорбции водорода на никеле, полученном восстановлением прокаленного при 300 в течение 30 час. В первой работе [7] автор указывает, что, работая в пределах давления порядка 35 - 50 мм, он установил три вида адсорбции. Быстрая адсорбция, равновесие которой устанавливается практически сразу; медленная адсорбция, равновесие этой адсорбции устанавливаются в течение 15 - 20 час. Во второй работе Дзидзима [7] указывает, что если катализатор прокаливать при все повышающихся температурах, то второй вид адсорбции устраняется. [49]
Медленный подъем кривой поляризации со временем ( см. рис. 3) с этой точки зрения объясняется тем, что вытеснение чужеродных частиц, а также адсорбция комплексных цианистых анионов происходит медленнее, чем процесс разряда ионов металла. При перерыве тока концентрация адсорбированных комплексных ионов на поверхности электрода увеличивается, вследствие чего при повторном включении тока процесс протекает при меньшей поляризации. По мере течения электролиза концентрация адсорбированных ионов падает и вследствие медленной адсорбции этих ионов поляризация повышается. Следовательно, скорость электрохимической реакции определяется скоростью адсорбции комплексных ионов. [50]
При фронтальной хроматографии концентрация исследуемог вещества в потоке газа-носителя у входа в колонну поддерживается постоянной и регистрируется нарастание его концентрации у выхода из колонны до величины, равной концентрации у входа в колонну. Меняя постоянную концентрацию адсорбата в газе-носителе, получают различные выходные кривые, представляющие зависимости концентрации адсорбата в выходящем из колонны газе от времени выхода. Анализ этих кривых позволяет в благоприятных случаях ( для не слишком медленной адсорбции) получить ряд точек или отрезков для построения изотермы адсорбции. Существенно выбрать оптимальные условия опыта - шаровидную форму, близкие размеры и возможно более однородную упаковку зерен адсорбента ( не содержащих тонких пор), температуру колонны и скорость потока газа, чтобы в наибольшей степени приблизиться к равновесию в колонне и иметь возможность вычислить равновесную изотерму адсорбции из выходных кривых. [51]
По нашим данным, для завершения медленной стадии хемосорб -, ции кислорода при давлении 0 07 мм рт. ст. требуется несколько суток. При повышении давления скорость медленной стадии увеличивается пропорционально jo0 52, [1,3] Этим можно объяснить изменение контактной разности потенциалов с увеличением давления. Изменение контактной разности потенциалов при завершении быстрой стадии меньше, чем соответствующее медленной адсорбции. Полученные данные позволяют сделать вывод, что при хемосорбции второго слоя атомов кислорода на поверхности германия образуется новое соединение. [52]
Предполагается, что адсорбированный слой при переходе из параболической области в линейную превращается из ненасыщенного в насыщенный. Так может получиться в том случае, если слабая, но быстрая адсорбция действует одновременно с сильной, но медленной адсорбцией. При низких температурах превалирует слабая и быстрая адсорбция, а сильная адсорбция остается несущественной. При высоких же температурах верна обратная картина. [53]
ОН - и ZnH-полос; обе они изменяются с ростом давления водорода при 30 С. Кружками обозначены наблюдения при давлениях 0; 0 1; 0 35; 2 3; 5 2; 13 0; 38 7 тор. Каждое измерение интенсивности заканчивалось не позднее чем через 15 мин после достижения данного давления; таким образом исключалось влияние последующей стадии медленной адсорбции. [54]
При кратком изложении выводов теории электронных переходов при хемосорбции отмечается важная роль потенциального барьера, связанного с двойным слоем между ионами, адсорбированными на поверхности, и ионизованными примесями противоположного заряда в полупроводнике. Показано также, что теория электронных переходов позволяет дать удовлетворительную интерпретацию многих аномальных кинетических эффектов на окиси цинка. Считая переход электрона лимитирующей стадией, удается объяснить медленные обратимые изменения электропроводности около 500 С, медленные обратимые и необратимые изменения электропроводности около 100 С, процессы медленного роста и падения фотопроводимости, изученные в основном в интервале от комнатной температуры до 100 С, и медленную адсорбцию водорода на окиси цинка. [55]
В переходной области скорость процесса определяется как диффузионными, так и кинетическими факторами. Таким образом, в общем случае суммарный коэффициент массопередачи зависит от скорости переноса молекул СС14 от наружной поверхности частиц вглубь пористой массы угля и скорости адсорбции молекул ССЦ на стенках пор угля. При этом определяющей является скорость наиболее медленного процесса. При медленной адсорбции суммарная скорость процесса не зависит от размера частиц и скорости потока. Коэффициент массопередачи определяется скоростью адсорбции, которая может быть рассчитана по законам химической кинетики. [56]
Страницы: 1 2 3 4