Диссимметрия
Cтраница 1
Диссимметрия может быть создана и на обычных катио-нитах путем сорбции на них оптически активных комплексов. Однако, в данном случае механизм сорбции отличается от лИ гандообмевнО ГО, так как обмен лигандов во внутренней сфере инертных комплексов Со ( 3) затруднен. Примером аналогичной ионной связи диссимметрического компонента с полимерным каркасом может служить анионит Дау-экс 1X4, нейтрализованный анионами тартрата. [1]
Диссимметрия при Сэ имеет решающее значение для асимметрического синтеза оксинитрилов. Уничтожение центра диссимметрии в положении 9 в молекуле катализатора, достигавшееся применением дезоксигидроцинхонина, дезоксигид-роцинхонидина, дезоксихинина и дезоксигидрохинидина, приводит к неактивному или малоактивному оксинитрилу. Конфигурация Gg в алкалоиде определяет и конфигурацию оптически активного оксинитрила. Алкалоид с L-конфигурацией при Сэ ( 9-зпихинин и 9-эпицинхонидин) вызывает образование и оксинитрила с L-конфигурацией. Исключение составляют только пиридилгексагидро-цинхонин и N-нитрозопиридилгексагидроцинхонин, что не удивительно, поскольку у этих алкалоидов появляется еще новый центр диссимметрии. [2]
Диссимметрия при С9 имеет решаю щее значение для асимметрического синтеза оксинитрилов Уничтожение центра диссимметрии в положении 9 в молекуле катализатора, достигавшееся применением дезоксигидроцинхонина. Кроме того, конфигурация С9 в алкалоиде определяет и конфигурацию оптически-активного оксинитрила. Исключение состав ляют только пиридилгексагидроцинхонин и N-нитрозопиридил-гексагидроцинхонин, что не удивительно, поскольку у этих алкалоидов появляется еще новый центр диссимметрии. [3]
Диссимметрия при С9 имеет решающее значение для асимметрического синтеза оксинитрилов. Уничтожение центра диссимметрии в положении 9 в молекуле катализатора, достигавшееся применением дезоксигидроцинхонина, дезоксигидроцинхонидина, дезоксихинина и дезоксигидрохиниди-на, приводит к неактивному или малоактивному оксинитрилу. Кроме того, конфигурация С9 в алкалоиде определяет и конфигурацию оптически-активного оксинитрила. Алкалоид с L-конфи-гурацией при С9 ( 9-эпихинин и 9-эпицинхонидин) вызывает образование и оксинитрила с L-конфигурацией. Исключение составляют только пиридилгексагидроцинхонин и N-нитрозопиридил-гексагидроцинхонин, что не удивительно, поскольку у этих алкалоидов появляется еще новый центр диссимметрии. [4]
Диссимметрию отрицательной и положительной частей можно объяснить нало жением перехода при 280 ммк. [6]
 |
Обозначения комплексов, диссимметричных вследствие несимметричности некоторых хелатов. [7] |
Если диссимметрия в комплексе вызвана только координацией асимметричного лиганда, то чтобы описать конфигурацию этого комплекса достаточно обычных обозначений для абсолютной конфигурации лиганда. Это справедливо, даже если лиганд становится асимметричным только в результате координации; например, абсолютная конфигурация комплексов [ Со ( МН3) 5 ( 5 - 1-фенилэтил-амин) ] 3 и [ Со ( МН3) 5 ( я-саркозин) ] 3 полностью описывается приведенными формулами. [8]
Термины диссимметрия, диссимметричный применяются для обозначь ния конфигурации индивидуальной молекулы или радикала, а термин асиь матричный относится к агрегатам диссимметричных молекул, обнаруживай щих оптическую активность, и к процессам, связанным с получением ил разложением таких агрегатов. [9]
Термины диссимметрия, диссимметричный применяются для обознач ния конфигурации индивидуальной молекулы или радикала, а термин аси метричный относится к агрегатам диссимметричных молекул, обнаружива ] щих оптическую активность, и к процессам, связанным с получением ш разложением таких агрегатов. [10]
 |
Оптическая схема фотометра Аминко, предназначенного для измерения светорассеяния. [11] |
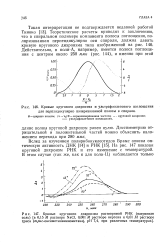
Измерения диссимметрии проводят в допускаемом интервале концентраций и результаты экстраполируют к нулевой концентрации. Отрезок, отсекаемый на оси / 45 Д 35, называют внутренней диссимметрией. [12]
Возникнуть же диссимметрия может по таким причинам: или молекула имеет спиралевидную структуру ( по словам Пастера, атомы могут быть сгруппированы, следуя поворотам правой ушной раковины) или атомы расположены в вершинах неправильного тетраэдра. [13]
Простейшей причиной диссимметрии органической молекулы является атом углерода, с которым связаны четыре других атома или грудры. [14]
Примеры превращения алленовой аксиальной диссимметрии в центровую диссимметрию меньше изучены по сравнению с асимметрическим переносом в обратном направлении, который рассматривался выше. В той мере, в какой известны механизмы таких реакций и конфигурации продуктов, эти превращения могут быть использованы для установления конфигурации в ряду алленов. [15]
Страницы: 1 2 3 4