Диссимметрия
Cтраница 3
 |
Стереохимия реакции расщепления карбанионов. [31] |
Лучшим доказательством, что несимметричная сольватация, а не диссимметрия как таковая, обусловливает сохранение активности в карбанионах, служит приведенное ранее наблюдение, что даже бензильные карбанионы способны сохранять оптическую активность. [32]
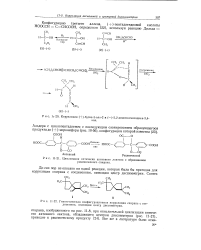 |
Циклизация оптически активного лактона с образованием рацемического спирана. [33] |
Гипотетическая конфигурационная корреляция спирана с соединением, имеющим центр диссимметрии. [34]
Следовательно, оптическая активность связана лишь с определенным видом диссимметрии ( см. 8.2.2), а именно с диссим-метрией, обусловливающей несовместимость объекта с его зеркальным отображением. Такой вид диссимметрии, как сказано выше, получил название хиральностъ. Хиральные объекты относятся друг к другу как правая и левая рука, или винт с правой и левой резьбой, т.е. они несовместимы в пространстве и представляются как зеркальные отображения друг друга. Оптически активная молекула хиральна, а оптически неактивная - ахираль-на, однако если молекулу нельзя совместить с ее зеркальным отображением, то зеркальное отображение соответствует другой, отличной молекуле, которую в принципе можно синтезировать. Удельное вращение ( [ а ] в формуле ( 1)) энантиомеров одинаково по абсолютной величине и противоположно по знаку: один энантиомер - левовращающий, а второй - правовращающий. Кроме знака вращения, все другие физические и химические свойства энантиомеров в газовой фазе, а также в ахиральных жидких средах одинаковы. Однако, если жидкая среда хиральна ( например, в раствор добавлен хиральный реагент или катализатор, или сам растворитель хирален), свойства энантиомеров начинают различаться. При взаимодействии с другими хиральными соединениями, отзывающимися на зеркальную изомерию молекул, энан-тиомеры реагируют с различными скоростями. [35]
 |
Диастереомеры, образованные DL - [ Coen3 ] 3 и о - [ Соох3 ] 3 -. [36] |
Однако у этих двух комплексов имеется два следующих источника диссимметрии: наличие асимметрического атома азота делает одну конформацию хелатного кольца более предпочтительной по сравнению с другой. [37]
Этот тип асимметрического синтеза заключается в создании нового центра диссимметрии внутри молекулы под влиянием ужи существовавшего ранее диссимметрического атома с последующей) его деструкцией. [38]
Этот тип асимметрического синтеза заключается в создани нового центра диссимметрии внутри молекулы под влиянием у существовавшего ранее диссимметрического атома с последующе его деструкцией. [39]
Аллены ( см. выше) представляют пример соединений с аксиальной диссимметрией. [40]
Метод двойного расщепления неприменим для определения оптической чистоты соединений, диссимметрия которых обусловлена замещением протия на дейтерий. С другой стороны, поскольку оптические вращения oc - дейтерированных первичных спиртов на два порядка ниже, чем у а-фенилмасляной кислоты, то вращение оптически активного а-дейтерированного первичного спирта после частичного кинетического расщепления будет слишком мало, чтобы его можно было бы измерить с точностью, достаточной для расчета оптической чистоты. [41]
Однако помимо точки зрения, основанной на действии материальных носителей диссимметрии, было высказано предположение, опирающееся на статистическое толкование процессов, ведущих к получению асимметрических молекул. [42]
Таким образом, в молекуле комплекса может существовать несколько источников диссимметрии, что приводит к диастереоизомерии. Диастереоизомеры, или диастерео-меры - это стереоизомеры, обладающие одними и теми же элементами диссимметрии; некоторые из них ( но не все) являются энантиомерными. [43]
Значительный интерес представляют асимметрические синтезы соединений, не обладающих центрами диссимметрии, оптическая активность которых обусловлена диссимметрией молекулы в целом. Примером таких соединений могут служить замещенные дифенила, бензольные кольца которых не лежат в одной плоскости вследствие стерических препятствий. [44]
 |
Схема октаэдрических трис-хелатных комплексов симметрии DS. [45] |
Страницы: 1 2 3 4