Форма - катализатор
Cтраница 2
ER - свободная и связанная с реагентом формы катализатора. [16]
ООО р В связи с такими большими объемными скоростями формы катализаторов и реакторов проектируются таким образом, чтобы перепад давления был невелик и не превышал 1ОО мм рт.ст. Общее давление может изменяться от атмосферного до более высоких значений, величины которых находятся в соответствии с параметрами следующих стадий процесса. В частности, обработка отходящего газа, образующегося при окислении аммиака, обычно проводится при давлениях 5 - 7 атм. [17]
В такой системе должно существовать динамическое равновесие между окисленной и восстановленной формами катализатора, причем положение равновесия определяется относительными скоростями реакций окисления и восстановления. [18]
Составить кинетическое уравнение процесса методом Боденштейна - Семенова и методом графов с учетом различия форм катализатора. Гидропероксид и олефин берутся в избытке по отношению к катализатору. [19]
Промышленные цинк-хромовые катализаторы изготовляют двумя способами, причем оба включают две стадии: приготовление кисной формы катализатора и восстановление его до активного состояния. [20]
Константы скорости ki и k2 характеризуют скорость установления прото-литического равновесия между кислотной и основной формами катализатора, &3 - скорость взаимодействия свободных радикалов - первичных продуктов электрохимического акта. При бимолекулярной реакции свободных радикалов регенерируется катализатор в своей основной форме В и выделяется молекула водорода. По Майрановскому, каталитический эффект наблюдается лишь в том случае, когда кислотная форма катализатора восстанавливается на электроде при более положительных потенциалах, чем донор протонов. [21]
Константы скорости kl и k2 характеризуют скорость установления прото-литического равновесия между кислотной и основной формами катализатора, &3 - скорость взаимодействия свободных радикалов - первичных продуктов электрохимического акта. При бимолекулярной реакции свободных радикалов регенерируется катализатор в своей основной форме В и выделяется молекула водорода. По Майрановскому, каталитический эффект наблюдается лишь в том случае, когда кислотная форма катализатора восстанавливается на электроде при более положительных потенциалах, чем донор протонов. [22]
Отдельные обозначения на рис. 64 могут быть неравноценны из-за неодинаковой надежности основных источников, изменений формы катализатора ( гомогенный или гетерогенный, элемент или соединение), различных значений рН и особенно из-за различий и колебаний в скорости катализа. Интервал скоростей разложения очень велик. Например, в одних и тех же условиях металлическая сурьма почти инертна, тогда как осмий и свинец могут вызвать разложение со скоростями, которые можно считать взрывоподобными. Наблюдаются градации интенсивности среди родственных элементов, например в ряду цинк, кадмий и ртуть. Наиболее резким является изменение от стабилизатора к активному катализатору при переходе от олова к свинцу. [23]
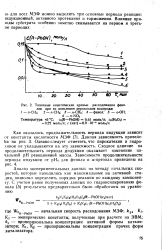 |
Типичные кинетические кривые расходования фено. [24] |
ЭВМ; & Р - пропорциональна концентрации активной формы катализатора; Ki, ICa - пропорциональны концентрации прочих форм катализатора. [25]
Мне хотелось бы также отметить, что значительное изменение свойств может происходить и у металлов в высокодисперсном состоянии, особенно в форме катализаторов на носителях. Носитель должен оказывать значительное влияние на структуру, а также, по-видимому, на развитие определенных кристаллических граней металла и на уровень Ферми. [26]
Каталитическое действие второй окислительно-восстановительной пары распространяется не только на некомплементарные реакции, поскольку скорость реакции окислителя и восстановителя с окисленной и восстановленной формами катализатора гораздо больше, чем скорость их прямой реакции. [27]
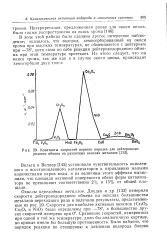 |
Константы скоростей первого порядка для дейтероводородного обмена на различных окислах металлов. [28] |
Вольтц и Веллер [145] установили чувствительность окисленного и восстановленного катализаторов к отравлению малыми количествами паров воды, и из величины этого эффекта вычислили, что площади активной поверхности обеих форм катализатора не превышают соответственно 2 % и 15 % от общей площади. [29]
Таким образом, в данной системе наблюдается катализ нитро-ксилами процесса окисления NOj до NO3 тетранитрометаном, а наблюдаемое в начальной стадии изменение [ R2NO ] соответствует установлению стационарного соотношения концентраций окисленной и восстановленной форм катализатора. [30]
Страницы: 1 2 3 4