Форма - катализатор
Cтраница 4
 |
Горизонталь - дении реакции в мелком бюксе ные зоны в реакции Бе - или внутри влажной фильтро-лоусова - Жаботинско - вальной бумаги могут возни-го в результате образо . [46] |
Очевидно, что химические превращения ионов катализатора Мл / М сопрягаются с основной реакцией окисления бромноватой кислоты. Поэтому в силу неустойчивости стадии автоускорения 1 при некоторых соотношениях между концентрациями реагентов даже в исходно гомогенной системе могут возникать осцилляции концентраций различных по степеням окисления форм катализатора, что в связи с их различной окраской легко детектируется визуально. [47]
Первое предпочтительней, поскольку трудно найти разбавитель, имеющий такую же форму и плотность, как катализатор. Форма катализатора ( и разбавителя) должна быть такой, чтобы слой катализатора не засорялся пылью. [48]
Первый случай наблюдается, например, для окисных катализаторов за счет обогащения или обеднения поверхности окисла кислородом по сравнению со стехнометрнческим составом, как то имеет место при разложении метанола па окиси цинка, или, что по сути тоже самое, за счет изменения концентрации анионных и катионных вакансий, как в реакции окисления СО на окислах марганца. Для кислотно-основных катализаторов такое влияние среды, как указывалось, связано с изменением функции кислотности поверхности от степени гидратации. Поскольку при реакциях гидратации-дегидратации имеет место равновесие гидратирован-ных и дегидратированных форм катализатора, а функция кислот ностн поверхности есть некоторая нелинейная функция от парциального давления водяного пара, то кинетическое уравнение реакции гидрации может иметь вид r - dC / dt & ( Я0) / [ Н2О ] Сп [ Н2О ] т, где п и т - эффективные порядки реакции по концентрациям субстрата и воды, а / [ Н2О ] - эмпирическая зависимость функции кислотности поверхности от парциального давления водяного пара. Очевидно, что, хотя в данном случае и не происходит фазового превращения катализатора, кинетика реакции может быть значительно усложнена. Аналогичные закономерности могут иметь место и при других видах влияния среды на поверхность катализатора. [49]
Поскольку выше было показано, что в реакции между гидроперекисью и солью металла образуются свободные радикалы, естественно принять, что основу этого процесса составляет механизм Габера - Вейсса. В начальный момент времени катализатор, CoSt2, находится в двухвалентной форме. Реакция двухвалентной соли с гидроперекисью приводит к образованию свободного радикала и трехвалентной формы катализатора. [50]
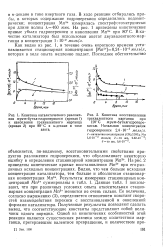 |
Кинетика каталитического разложе - [ IMAGE ] Кинетика восстановления. [51] |
На рис. 2 приведены кинетические кривые восстановления Мп3 при его различных исходных концентрациях. Данные табл. 1 показывают, что при различных условиях опыта относительная стационарная концентрация Мп3 меняется не очень сильно. Ее величина, согласно выражению ( 3), определяется отношением констант скоростей взаимодействия перекиси с восстановленной и окисленной формами катализатора. Полученные результаты позволяют сделать вывод, что соответствующие константы представляют собой величины одного порядка. [52]
Концентрацию катализатора можно определять по длительности индукционного периода, по истечении которого скорость реакции становится заметной. Этот способ является разновидностью метода фиксированной концентрации. Индукционный период наблюдается не только в реакциях Ландольта, но и в автокаталитических реакциях, а также в реакциях, когда в их начальный период изменяется соотношение форм катализатора. [53]
Это уравнение было подтверждено на опыте [27] на примере каталитической волны, вызываемой пиридином в боратных буферных растворах. Приведенная выше схема реакций была также описана соответствующими дифференциальными уравнениями, которые были решены методом безразмерных параметров [29], а в последующей работе [79] полученные при этом соотношения были сопоставлены с уравнениями, выведенными приближенным методом. В той же работе [79] приведены уравнения каталитических волн для различных соотношений между скоростями реакций ( XI) и ( XIII) и для различных значений равновесия между кислотной и основной формами катализатора в растворе. [54]
Обнаруженная зависимость / на, от концентрации катализатора указывает на сложный характер взаимодействия гидроперекиси с ацетатом двухвалентного кобальта. В литературе существует предположение, что взаимодействие ROOH с металлом переменной валентности осуществляется последовательно в две стадии: в первой стадии за счет бимолекулярной реакции гидроперекиси с ацетатом двухвалентного кобальта равновесно образуется комплекс гидроперекиси с ацетатом двухвалентного кобальта. Для объяснения квадратичной зависимости w от [ СоАс2 ] предполагается [276], что во второй стадии процесса при взаимодействии образовавшегося комплекса со второй молекулой катализатора происходит распад гидроперекиси с образованием свободного радикала и трехвалентной формы катализатора. [55]
Страницы: 1 2 3 4