Диссоциация - молекула - кислород
Cтраница 2
Энтальпия образования оксида углерода ( II) равна - 26 42 ккал / моль, энтальпия возгонки графита 166 ккал / моль, энергия диссоциации молекул кислорода 118 ккал / моль. [16]
Даже для реакции углерод - кислород, протекающей в условиях первого порядка, сомнительно, чтобы концепция Россбер-га имела какое-либо значение, так как, по-видимому, не оправданно сравнивать половину величины энергии диссоциации молекулы кислорода с энергией активации реакции. Ясно, что величина энергии активации будет одной и той же независимо от того, выражена ли скорость реакции в молях или через число атомов кислорода, реагирующих в единицу времени. [17]
В том, что с точки зрения существующих данных об энергии разрыва атомных связей первоначальное образование перекисей при окислении углеводородов более вероятно, так как должно происходить при более низкой температуре, чем возникновение гидро-ксильных соединений, требующее предварительной диссоциации молекулы кислорода на атомы. [18]
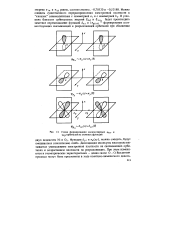 |
Схема формирования молекулярных цпх - и яу-орбиталей из атомных функций. [19] |
Функции dyz и гги ( ху), можно ожидать, будут смешиваться относительно слабо. Диссоциация молекулы кислорода вызывается уменьшением электронной плотности на связывающих орби-талях и возрастанием плотности на разрыхляющих. При этом изменяются и геометрические характеристики - длина связи О - О. [20]
Информация о механизме каталитической реакции между паром и углем очень ограничена. Металлы способствуют диссоциации молекул кислорода: и активации атомов углерода. [21]
Озон ( 03) образуется в верхних слоях атмосферы под действием ультрафиолете вого света, излучаемого солнцем. Первой стадией образования озона является диссоциация молекулы кислорода на два атома кислорода; каждый из атомов кислорода после этого соединяется с молекулой кислорода и образует молекулу озона. Энергия диссоциации молекулы кислорода на атомы кислорода составляет 5 08 эв. [22]
Высокая теплота адсорбции дает право считать, что процесс сопровождается большим изменением изобарного потенциала. Освобождение значительного количества энергии делает возможной диссоциацию молекул кислорода на атомы и адсорбцию их с образованием химических связей, что оказывается энергетически выгодным. [23]
Некоторые сторонники перекисной теории ( см. ниже) считают теорию гидроксилирования вообще несостоятельной. Они указывают, что для принятия ее необходимо допустить предварительную диссоциацию молекул кислорода на атомы, так как непонятно, каким образом реагирует молекулярный кислород. Допущение же диссоциации О2 zi 2 ( 5 неприемлемо, так как ни энергетически, ни экспериментально это необосновано. Однако некоторые факты не оправдывают столь резкой критики, так как в определенных условиях при окислении углеводородов могут получаться и спирты ( например, при холрднопламенном окислении, стр. Все же остается неясным вопрос, являются ли последние первичными продуктами окисления углеводородов или же они образуются в результате вторичных реакций. [24]
Некоторые сторонники перекисной теории ( см. ниже) считают теорию гидроксилирования вообще несостоятельной. Они указывают, что для принятия ее необходимо допустить предварительную диссоциацию молекул кислорода на атомы, так как непонятно, каким образом реагирует молекулярный кислород. Допущение же диссоциации О, jz 2O неприемлемо, так как ни энергетически, ни экспериментально это необосновано. Однако некоторые факты не оправдывают столь резкой критики, так как в определенных условиях при окислении углеводородов могут получаться и спирты ( например, при холоднопламенном окислении, стр. Все же остается неясным вопрос, являются ли последние первичными продуктами окисления углеводородов или же они образуются в результате вторичных реакций. [25]
На фронте воздушной УВ большой интенсивности ( в ближней зоне действия взрыва) термодинамические параметры довольно высоки и определяют неравновесные процессы в ударно-сжатом воздухе. При повышении температуры возбуждаются внутренние степени свободы молекул, происходят диссоциация молекул кислорода и азота, образование окислов азота и других продуктов реакции, электронное возбуждение и ионизация различных компонентов воздуха. [26]
На фронте воздушной УВ большой интенсивности ( в ближней зоне действия взрыва) термодинамические параметры довольно высоки и определяют неравновесные процессы в ударно сжатом воздухе. При повышении температуры возбуждаются внутренние степени свободы молекул, происходят диссоциация молекул кислорода и азота, образование окислов азота и других продуктов реакции, электронное возбуждение и ионизация различных компонентов воздуха. [27]
Благодаря значительному сродству платины к кислороду при достаточной устойчивости кристаллической решетки поверхность платины способна связывать кислород с силой, достаточной для разрыва связи в молекуле кислорода, причем способность кислорода к взаимодействию с окисляющимися веществами сохраняется. Таким путем сглаживается высокий энергетический барьер, обусловливаемый при окислительных реакциях высокой энергией диссоциации молекул кислорода. [28]
На высотах более 100 км происходит изменение процентного содержания отдельных газов, связанное с их диффузным расслоением под влиянием гравитации и температуры. Кроме того, под действием коротковолновой части ультрафиолетовых и рентгеновых лучей на высоте 100 км и более происходит диссоциация молекул кислорода, азота и углекислого газа на атомы. На больших высотах эти газы находятся в виде сильно ионизированных атомов. [29]
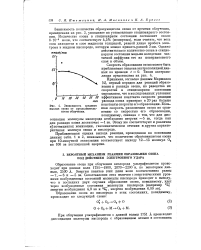 |
Зависимость среднего выхода озона от продолжительности облучения. [30] |
Страницы: 1 2 3 4