Диссоциация - растворенное вещество
Cтраница 3
Энергетические характеристики и свойства растворов, связанные с диссоциацией растворенных веществ, описаны в следующем разделе. [31]
Коэффициент распределения используется для экспериментального определения степени ассоциации пли диссоциации растворенного вещества в том или ином растворителе, активности растворенных веществ и других подобных величин. [32]
Электропроводность растворов обусловлена присутствием в них ионов, образующихся при диссоциации растворенных веществ. В водном растворе под действием молекул воды хлористый водород хорошо диссоциирует на ионы, поэтому такой раствор обладает значительной электропроводностью. [33]
Причиной отклонения закона распределения от прямолинейности может быть ассоциация или диссоциация растворенного вещества в одной или в обеих фазах. [34]
Экспериментальное исследование коэффициентов распределения может служить для определения степени ассоциации или диссоциации растворенного вещества в том или ином растворителе, константы равновесия реакции, протекающей в одной из фаз, и тому подобных величин. [35]
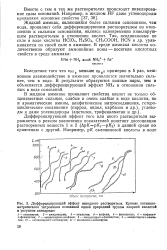 |
Дифференцирующий эффект неводного растворителя. Кривые потенцио-метрического титрования оснований одной природной группы хлорной кислотой в уксусном ангидриде. [36] |
Дифференцирующий эффект того или иного растворителя выражается в резком увеличении показателей констант диссоциации растворенных веществ 1 и 2 ( ApKpKi - pK2) в данной среде по сравнению с другой. [37]
Одним из важнейших понятий классической теории электролитической диссоциации является понятие о степени диссоциации растворенного вещества. [38]
При рассмотрении влияния растворителя ( среды) на величины коэффициента активности и константы диссоциации ионизирующего растворенного вещества следует различать первичный и вторичный эффекты среды. В случае раствора электролита, в котором присутствуют нейтральные ( неводные) молекулы, суммарный эффект среды определяется как логарифм-отношения коэффициента активности электролита в присутствии нейтральных молекул к коэффициенту активности в чистой воде при той же концентрации электролита. Оба коэффициента активности в этом отношении отнесены к единице, как к коэффициенту активности при бесконечном разбавлении в чистой воде. Первичным эффектом среды обозначают тот предел, к которому приближается суммарный эффект, когда концентрация электролита стремится к нулю. Вторичный эффект среды всегда определяется как разность между суммарным и первичным эффектами. [39]
При рассмотрении влияния растворителя ( среды) па величины коэффициента активности и константы диссоциации ионизирующего растворенного вещества следует различать первичный и вторичный эффекты среды. В случае раствора электролита, в котором присутствуют нейтральные ( неводпые) молекулы, суммарный эффект среды определяется как логарифм отношения коэффициента активности электролита в присутствии нейтральных молекул к коэффициенту активности в чистой воде при той же концентрации электролита. Оба коэффициента активности в этом отношении отнесены к единице, как к коэффициенту активности при бесконечном разбавлении в чистой воде. Вторичный эффект среды всегда определяется как разность между суммарным и первичным эффектами. [40]
Закон Вант-Гоффа хорошо оправдывается только для таких слабых растворов, в которых не происходит диссоциации растворенного вещества. Для диссоциированных растворов ( электролитов) осмотическое давление оказывается значительно большим, чем следует по закону Вант-Гоффа. Это объясняется тем, что при диссоциации увеличивается число частиц растворенного вещества ( из одной молекулы могут образоваться два иона) и, следовательно, согласно формуле ( 11), увеличивается осмотическое давление. [41]
Поправки эти, однако, обычно малы, если только не происходит ассоциации или диссоциации растворенного вещества. [42]
АГзам - понижение температуры замерзания раствора, вычисленное по уравнению (VII.11) в предположении отсутствия диссоциации растворенного вещества; АГкип - повышение температуры кипения раствора, вычисленное по уравнению ( VII. Ар / р - относительное понижение давления пара растворителя над раствором в предположении отсутствия диссоциации растворенного вещества; АТ аам ( оп) - опытное понижение температуры замерзания раствора, если растворенное вещество в растворе диссоциирует; А Угашал) - опытное повышение температуры кипения, если растворенное вещество в растворе диссоциирует: ( Ap / Pi) 0n - относительное понижение давления пара растворителя над раствором, полученное опытным путем, если растворенное вещество в растворе диссоциирует. [43]
В начале этой главы мы указали, что сильные и слабые электролиты различаются по степени диссоциации растворенного вещества на ионы. В соответствии с этим кислоты можно различать по концентрации ионов водорода в растворе, что позволяет количественно сравнивать силу кислот. [44]
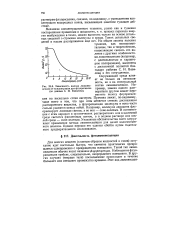 |
Зависимость выхода люминесценции от концентрации для флуоресцеина ( по данным С. И. Вавилова. [45] |
Страницы: 1 2 3 4