Функция - гиббс
Cтраница 1
Функция Гиббса для идеального газа ( на один моль его) выражается уравнением ( ХП. [1]
Функция Гиббса для реакции равна - 237 19 кДж / моль при 298 К. [2]
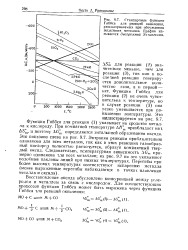 |
Стандартные функции Гнббса для реакций окисления, рассматриваемых при обсуждении выделения металлов. График называется диаграммой Эл гингхэма. [3] |
Функция Гиббса для реакции ( 2) не очень чувствительна к температуре, но в случае реакции ( 3) она резко уменьшается при повышении температуры. [4]
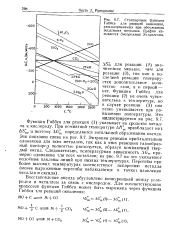 |
Стандартные функции Гнббса для реакций окисления, рассматриваемых при обсуждении выделения металлов. График называется диаграммой Эл гингхэма. [5] |
Функция Гиббса лая реакции ( 1) указывает на сродство металла к кислороду. & S m, и поэтому АС, определяется энтальпией образования оксида. Это показано слева на рис. 9.7. Энтропия реакции приблизительно одинакова для всех металлов, так как в этих реакциях газообразный кислород полностью расхотуется, образуя компактный твердый оксид. Следовательно, температурная зависимость AGm примерно одинакова vifl всех металлов; на рис. 9.7 на это указывают подобные наклоны линий при низких температурах. [6]
Как функция Гиббса зависит от температуры. [7]
Как функция Гиббса зависит от давления. Уравнение (6.2.3) показывает, что знания объема системы достаточно для предсказания зависимости G от давления. Поскольку V должен быть положительным, С возрастает с увеличением давления в системе. [8]
Изменение функции Гиббса отождествляем с электрической работой ( гс е) заряжения ионов, находящихся в их конечном распределении. [9]
Изменение функции Гиббса ( свободной энтальпии) в некоторой химической реакции является весьма важной характеристикой, поскольку, как мы видели при изучении термодинамической доступности энергии ( гл. [10]
TS есть функция Гиббса. [11]
Для нахождения функции Гиббса воспользуемся теоремой § 13.2. Сначала вычислим для твердого тела с одной неподвижной точкой. [12]
Вычисления изменений функции Гиббса, или свободной энергии, дают возможность делать обоснованные выводы о способности химических реакций к самопроизвольному протеканию. [13]
Иллюстрацией важности функции Гиббса в определении направления спонтанного химического изменения является существование эндотермических реакций ( стр. Например, при растворении п гюче хлористого аммония при 25 С ДЯ5т 34 7 кЧж / моль, однако растворение происходит спонтанно. [14]
В обозначении молярной функции Гиббса g - знак тильда используется для напоминания о том, что Я; и S - имеют специальные точки отсчета, что дает возможность согласовать эти величины друг с другом и с изменениями энтальпии и энтропии в реакции. [15]
Страницы: 1 2 3 4