Диссоциация - вода
Cтраница 2
Диссоциация воды возрастает с температурой. [16]
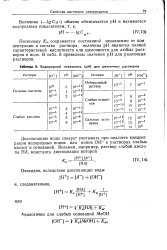 |
Водородный показатель ( рН для различных растворов. [17] |
Диссоциацию воды следует учитывать при подсчете концентрации водородных ионов или ионов ОН - в растворах слабых кислот и оснований. [18]
Диссоциацию воды, как известно, приходится учитывать в процессах гидролиза, электролиза и в ряде других случаев. [19]
 |
Водородный показатель ( рН для различных растворов. [20] |
Диссоциацию воды следует учитывать при подсчете концентрации водородных ионов или ионов ОН - в растворах слабых кислот и оснований. [21]
Диссоциацию воды, как известно, приходится учитывать в процессах гидролиза и в ряде других случаев. [22]
 |
Шкала рН для различных растворов. [23] |
Диссоциацию воды следует учитывать при подсчете концентрации водородных ионов или ионов ОН - в растворах слабых кислот и оснований. [24]
Диссоциацией воды объясняется важное явление - гидролиз солей. [25]
Диссоциацией воды на ионы объясняется явление гидролиза многих солей. [26]
Эта диссоциация воды обусловливает то явление, которое нами было описано на стр. ОН несвязанными, сколько обыкновенно содержится в воде. Этот остаток для солей сильных кислот и сильных оснований в расчет не принимается, напротив, он принимается в расчет для солей очень слабых кислот или оснований, в силу следующих причин. [27]
Поскольку диссоциация воды - эндотермический процесс, то с ростом температуры она усиливается, и значение / Сн2о возрастает. [28]
 |
Влияние температуры на Кш. [29] |
При диссоциации воды также образуются гидроксил-ионы и в равных количествах ионы водорода. [30]
Страницы: 1 2 3 4