Диссоциация - вода
Cтраница 4
Константа диссоциации воды сильно зависит от температуры, так pKw 14 2 при 18 С и 12 2 при 100 С. В разбавленных растворах щелочи рОН не изменяется при нагревании, в то время как рН уменьшается. Поэтому фенолфталеин, имеющий интервал перехода окраски при рН 8 3 - т - 10 0, при нагревании обесцвечивается. [46]
Уравнение диссоциации воды, учитывающее образование положительного иона Н О и отрицательного ОН -, указывает на суть процесса. Та молекула, которая теряет протон является донором протона, а та, которая приобретает протон, - его акцептором. Утверждение, что одни молекулы воды являются донорами, а другие акцепторами, конечно, формально. [47]
Константа диссоциации воды увеличивается при повышении температуры в большей степени, чем константы диссоциации продуктов гидролиза - слабых кислот и оснований, поэтому при нагревании степень гидролиза возрастает. К этому выводу легко прийти и иначе: так как реакция нейтрализации экзотер-мична, то гидролиз, будучи противоположным ей процессом, эндотермичен, поэтому в соответствии с принципом Ле Шателье нагревание вызывает усиление гидролиза. [48]
Состояние диссоциации воды зависит также от растворенных в ней кислот и оснований. Гидратированный протон, который обычно обозначается Н и называется ионом гвдрония, имеет, как уже указывалось, большую энергию гидратации. [49]
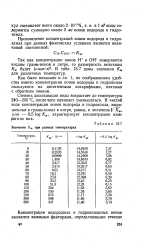 |
Значения Kw ПРИ разных температурах. [50] |
Степень диссоциации воды возрастает до температуры 240 - 250 С, после чего начинает уменьшаться. В чистой воде концентрации ионов водорода и гидроксила, выраженные в грамм-ионах в литре, равны, и величина KW, или - 0 5 log Kw, характеризует концентрацию каждого из них. [51]
 |
Изменение рН пермеата при раз - рН делении обратным осмосом растворов некото-рых хлоридов металлов. [52] |
Особенность диссоциации воды при разделении растворов электролитов обратным осмосом или электроосмофильтрацией заставляет во многом пересмотреть существующие модели ионного транспорта через мембраны. Очевидно, указанное явление необходимо учитывать при теоретическом описании переноса ионов в процессе электроосмофильтрации. Явление диссоциации воды на границе разделяемого раствора и мембраны в данном случае исключает правомерность указанного подхода, так как природа разложения воды обусловливает отклонение состава раствора, примыкающего к этой границе, от термодинамически равновесного. [53]
Степень диссоциации воды а1 8 - 10 - 9, что составляет очень небольшую величину. Так, из 556 000 000 молекул Н2О в диссоциированном состоянии при комнатной температуре в среднем находится лишь одна. Несмотря на это, ионизация воды имеет большое значение. [54]
Степень диссоциации воды а1 8 10 - 9, что составляет очень небольшую величину. Так, из 556 000 000 молекул FbO в диссоциированном состоянии при комнатной температуре в среднем находится лишь одна. Несмотря на это, ионизация воды имеет большое значение. [55]
Константа диссоциации воды применяется главным образом в теории кислот и оснований для сравнения с константами диссоциации других соединений ( разд. [56]
Степень диссоциации воды при очень высоких давлениях служила объектом многочисленных исследований. Ионное произведение активности воды Kw, измеренное при 25 С и при давлении 200 МПа, оказалось в 4 раза большим, чем при атмосферном давлении; при давлении же, равном 800 МПа, эта величина возросла в 51 3 раза. Особенно сильно возрастает Kw при одновременном действии высоких давлений и температур. Правда, в таких условиях воду уже нельзя считать жидкой фазой - давления и температуры соответствуют закритической области. [57]
Страницы: 1 2 3 4