Диссоциация - хлор
Cтраница 2
Очевидно, что практическое значение может иметь только диссоциация хлора, молекула которого менее прочна: для него теплота диссоциации QD241 кДж / моль, тогда как для водорода QD 436 кДж / моль. Химическая реакция приводит к появлению в системе атомарного водорода; его стационарная концентрация, определяемая уравнением (1.14), меньше концентрации атомарного хлора, но значительно превосходит равновесную для диссоциации водорода. [16]
При медленной реакции в нагретом сосуде устанавливается равновесие диссоциации хлора по гетерогенному механизму в течение времени, малого по сравнению со временем заметного превращения. После этого периода нестационарной диссоциации скорость реакции не зависит от материала реактора ( катализатор не влияет на состояние равновер: ия), хотя влияние стенок ускорило достижение стационарного режима. [17]
При медленной реакции в нагретом сосуде устанавливается равновесие диссоциации хлора по гетерогенному механизму в течение времени, малого по сравнению со временем заметного превращения. После этого периода нестационарной диссоциации скорость реакции не зависит от материала реактора ( катализатор не влияет на состояние равновевия), хотя влияние стенок ускорило достижение стационарного режима. [18]
При медленной реакции в нагретом сосуде устанавливается равновесие диссоциации хлора по гетерогенному механизму в течение времени, малого по сравнению со временем заметного превращения. После этого периода нестационарной диссоциации скорость реакции не зависит от материала реактора ( катализатор не влияет на состояние равновесия), хотя влияние стенок ускорило достижение стационарного режима. [19]
При взаимодействии хлора с водородом в нагретых сосудах равновесие диссоциации хлора устанавливается на стенках в течение времени, малого по сравнению со временем заметного превращения. При распространении пламени время реакции мало, тогда как сам процесс протекает в пространстве без стенок, катализирующих диссоциацию хлора. Атомарный хлор может в этом случае образовываться только при гомогенных реакциях. [20]
Фрост и Макдауэл [197] на основании данных по ионизации и диссоциации хлора, брома, иода, хлорида и бромиода построили кривые потенциальной энергии, иллюстрирующие процессы образования наблюдаемых отрицательных ионов. [21]
При термическом хлорировании, протекающем обычно в газовой фазе, диссоциация хлора на атомы наблюдается при 300 - 400 С. [22]
К сожалению, исходя из этой величины, а также теплот диссоциации хлора и монофторида хлора, величина теплоты диссоциации фтора составляет 33 4 или 30 6 ккал. Эти значения настолько меньше обычно принятой величины теплоты диссоциации фтора ( 62 6 ккал), что для выяснения этого вопроса необходимы дальнейшие исследования. [23]
Обрыв цепей и при рекомбинации на стенках, и тройных соударениях в объеме не препятствует установлению равновесия диссоциации хлора. [24]
 |
Зависимость выхода этиленхлоргидрина от температуры при гипо-хлорировании этилена различной степени дробления. [25] |
В условиях промышленного гипохлорирования этилена выход этиленхлоргидрина зависит практически от двух основных факторов - растворимости этилена и степени диссоциации хлора. [26]
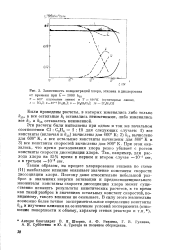 |
Зависимость концентраций хлора, этилена И дихлорэтана от времени при к 1000 к1ъ. [27] |
Таким образом, на процесс хлорирования этилена по схеме ( 11) наибольшее влияние оказывает значение константы скорости диссоциации хлора. Поэтому даже относительно небольшой разброс в значениях энергии активации и предэкспоненциального множителя константы скорости диссоциации хлора может существенно исказить результаты кинетических расчетов, в то время как такой разброс в значениях остальных констант скоростей, по-видимому, такого влияния не оказывает. [28]
На рис. 5 представлены кривые, полученные для температур 600 и 800 К при отношении С12: С2Н4 1: 10 для константы диссоциации хлора, увеличенной по сравнению с вычисленной по формуле ( 16) в 1000 раз, что соответствует энергии активации при 600 К - 39 7 ккал / молъ, а при 800 К - 37 ккал / молъ. [29]
В смесях с избытком водорода ( у0 5) активные центры генерируются в узкой зоне вблизи Ть - При более низких температурах скорость диссоциации хлора, связанной с преодолением высокого энергетического барьера, быстро падает до нуля; по другую сторону зоны генерирования продукты сгорания не содержат исходного компонента - свободного хлора. [30]
Страницы: 1 2 3 4