Диссоциация - карбоксильная группа
Cтраница 1
Диссоциация карбоксильных групп с отделением протона протекает легко, вследствие чего комплексоны являются довольно сильными кислотами. При этом соответствующие константы диссоциации имеют очень близкие значения. Кислотная диссоциация бетаина протекает даже в щелочной области. [1]
Диссоциация карбоксильных групп аминокислоты в присутствии сильных кислот подавлена. [2]
Вследствие диссоциации карбоксильных групп мицеллы обладают отрицательным зарядом и окружены ионами противоположного знака или прикрепляются к положительно заряженным центрам в кристаллической структуре минералов. При перемещении флюидов в горных породах ( при движении неполярных жидкостей) возникает естественный фильтрационный потенциал и связанное с ним электрическое поле, в котором в природных условиях мицеллы могут перемещаться. По мнению В.А. Королева и других, этот механизм особенно эффективен в тонкопоровых разностях пород. [3]
Теплота диссоциации карбоксильных групп близка к нулю, а имидазольных составляет - 6 ккал / молъ, поэтому температурное поведение двух рассматриваемых ветвей кривой существенно различается и позволяет отличить конец титрования карбоксильных групп от начала титрования имидазольных. Поскольку теплота ионизации ( ДЯ-11 ккал / моль) а-аминогрупп ( титрующихся в конце нейтральной части кривой титрования) близка к теплоте ионизации е-аминогрупп ( титрующихся в щелочной области рН), то этот метод не может использоваться для разделения указанных областей кривой титрования. Щелочная часть кривой титрования на рис. 10 зависит от времени. Это, как указывалось выше, свидетельствует о наличии конформационных изменений под действием рН и может быть связано с влиянием рН на ионизацию тирозиновых остатков, заблокированных внутри белковой глобулы. Во всех случаях они отражают конформационную перестройку молекул, и исследование разностных кривых титрования позволяет получить некоторую информацию о характере такой перестройки. [4]
Теплота диссоциации карбоксильных групп близка к нулю, а имидазольных составляет - 6 ккал / молъ, поэтому температурное поведение двух рассматриваемых ветвей кривой существенно различается и позволяет отличить конец титрования карбоксильных групп от начала титрования имидазольных. Поскольку теплота ионизации ( А / / - 11 ккал / молъ) а-аминогрупп ( титрующихся в конце нейтральной части кривой титрования) близка к теплоте ионизации е-аминогрупп ( титрующихся в щелочной области рН), то этот метод не может использоваться для разделения указанных областей кривой титрования. Щелочная часть кривой титрования на рис. 10 зависит от времени. Это, как указывалось выше, свидетельствует о наличии конформационных изменений под действием рН и может быть связано с влиянием рН на ионизацию тирозиновых остатков, заблокированных внутри белковой глобулы. Во всех случаях они отражают конформационную перестройку молекул, и исследование разностных кривых титрования позволяет получить некоторую информацию о характере такой перестройки. [5]
В ледяной уксусной кислоте диссоциация карбоксильной группы аминокислот полностью подавляется, что позволяет титровать аминогруппу хлорной кислотой. [6]
Подобно тому как на диссоциацию карбоксильной группы влияют, заместители, они влияют и на диссоциацию группы ОН в фенолах. [7]
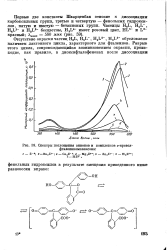 |
Спектры поглощения анионов и комплексов о-крезол-фталеинкомплексона. [8] |
Первые две константы Шварценбах относит к диссоциации карбоксильных групп, третью и четвертую - фенольных гидрокси-лов, пятую и шестую - бетаиновых групп. [9]
При добавлении к раствору белка слабой кислоты диссоциация карбоксильных групп в белковых молекулах подавляется, и в конечном счете в белке будет достигнуто равенство положительных и отрицательных зарядов. В зависимости от числа и природы основных и кислых групп в белке такое состояние достигается при разных концентрациях водородных ионов. [10]
На первой стадии диссоциация кислоты NH3RCO2H есть диссоциация карбоксильной группы кислоты, в то время как на второй стадии диссоциирует аммонийный ион. [11]
В общем случае глубина обесцвечивания определяется степенью диссоциации карбоксильных групп и растворимостью гидроксидных комплексов, а оптимум значений рН ( рис. VI.8) - соотношением между числом диссоциированных карбоксильных групп и количеством малорастворимых продуктов гидролиза коагулянта. Некоторое несоответствие значений экспериментально найденных оптимальных рН и рассчитанных с помощью уравнения (VI.6) может быть объяснено или неравновесным состоянием системы, или погрешностями расчета, связанными с недоучетом влияния других параметров. [12]
 |
Вытеснение аланина с может быть в известной мере сульфосмолы СДВ-3 раствором НС1. уменьшено при использова. [13] |
Далее, известно [39], что степень диссоциации карбоксильных групп аминокислот и пептидов уменьшается при замене воды ацетоном. Как видно из табл. 2, в соответствии с этим увеличивается сорбируемость аминокислот катионитом в солевой форме при переходе к ацетоновым растворам. [14]
Реакция амфотерного иона с кислотой фактически равноценна подавлению диссоциации карбоксильных групп. [15]
Страницы: 1 2 3 4