Диссоциация - карбоксильная группа
Cтраница 3
Сопоставление констант диссоциации органических кислот позволяет раскрыть индуктивное влияние заместителей на силу кислот, обусловленную диссоциацией карбоксильной группы. Влияние атома хлора через углеродную цепь на карбоксильную группу усиливает протони-зацию атома водорода этой группы и тем самым увеличивает диссоциацию кислоты. [31]
Добавляя к раствору белка кислоту и повышая тем самым концентрацию Н ионов в растворе, можно подавить диссоциацию карбоксильных групп белка и тем самым уменьшить его отрицательный заряд. [32]
Добавляя к раствору белка кислоту и повышая тем самым концентрацию Н ионов в растворе, можно подавить диссоциацию карбоксильных групп белка и тем самым уменьшить его отрицательный заряд. [33]
 |
Диффузионные потенциалы Е и числа переносов гс хлорид-ионов через пленки на основе различных полимеров в растворах КС1 разной концентрации. [34] |
Исходя из литературных данных, можно предположить, что у алкидных пленок появление отрицательного заряда связано с диссоциацией карбоксильных групп и переходом ионов водорода в раствор. [35]
На рис. 5.7 выделены три характерных участка: I - при рН3 0, в пределах которого степень диссоциации карбоксильных групп клеточной поверхности равна нулю ( клетка не заряжена), а аминогруппы флокулян-тов полностью диссоциированы. [36]
Объяснение малой скорости сорбции стрептомицина и других катионов карбоксильными катио-нитами в Н - форме следует искать в малой степени диссоциации карбоксильных групп, которая, естественно, приводит к малой скорости диффузии ионов водорода из ионита в раствор. [37]
Взаимодействие гуминовых кислот с сильными основаниями приво-датнк-йонизации карбоксильных, а затем фенольных груна Дня-большинства торфов и бурБ1Х углей значения констант диссоциации карбоксильных групп равны 10 4 - 10 5, для фенольных групп 10 9 - 10 - 10, что типично для алифатических и ароматических кислот и фенолов. [38]
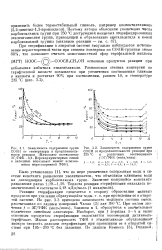 |
Зависимость содержания групп [ IMAGE ] Зависимость содержания групп СООН от температуры л продолжитель. [39] |
Было установлено [1], что по мере увеличения содержания воды в системе константа равновесия увеличивается, что объяснили влиянием воды на диссоциацию карбоксильных групп. [40]
Как видно из рис. 1, в отличие от смолы КБ-4П-2, на которой обмен катионов становится заметным только при рН 3, соответствующем началу диссоциации карбоксильных групп, обмен на окисленных углях происходит уже в гораздо более кислых растворах - при рН1 - 2 1 что прямо указывает на наличие на поверхности этих сорбентов гораздо более кислых групп, чем обычные карбоксильные. [41]
Если теперь раствор белка, находящегося в изоэлектрическом пункте, сильно подкислять какой-нибудь кислотой, например соляной, и тем самым сдвигать рН среды от изоэлектричеокого пункта в кислую сторону, то соляная кислота, как более сильная, подавит диссоциацию карбоксильных групп. [42]
Карбоновые кислоты относятся к числу сравнительно слабых кислот; в водном растворе они диссоциируют в ограниченной степени. При диссоциации карбоксильной группы отрицательный заряд распределяется по обоим атомам кислорода. [43]
Это обусловливается высокой жесткостью макромолекул по-лиамидокислоты и сольватацией их с растворителем. Вследствие диссоциации карбоксильных групп в системах, не содержащих LiBr, наблюдается более заметное р асширение клубка, чем в растворах с LiBr. Полиамидокислота с Мш 75000 в растворе диметилацет-амида с LiBr имеет. В системах, содержащих LiBr, с увеличением разбавления наблюдается возрастание оптической анизотропии. Это приводит к увеличению соотношения осей в эллипсоиде. При добавлении триэтиламина к разбавленным растворам полиамидокислоты происходит сильное возрастание вязкости. [44]
Шерстяное волокно окрашивается анионными красителями в кислой среде. При этих условиях диссоциация карбоксильной группы шерсти ослаблена, а аминогруппы, присоединив протон, превращаются в ионы аммония, количество которых находится в прямой зависимости от рН красильного раствора. Краситель в воде диссоциирован и его анион электролитически связывается с шерстью за счет ионов аммония. [45]
Страницы: 1 2 3 4