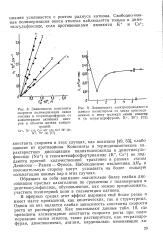
Слабая диссоциация
Cтраница 1
Слабая диссоциация связана с сильной кислотностью среды. [1]
Вследствие слабой диссоциации связи Sn-S образование оловоорганических сульфидов происходит даже в том случае, когда образуются хорошо, растворимые продукты реакции. Например, сульфиды быс - ( триалкил) -, диалкил -, трикумил - и дикумилолова получены [20, 122, 219-222] обменом сульфидов натрия или аммония с раствором ( или суспензией) оловоорганических галогенидов в воде. [2]
Ввиду сравнительно слабой диссоциации уксусной кислоты концентрация и ионов CHjCOO, и ионов № сильно понизится. [3]
Ввиду сравнительно слабой диссоциации уксусной кислоты концентрация и ионов СН3СОО, и ионов Н сильно понизится. [4]
Ввиду сравнительно слабой диссоциации уксусной кислоты концентрации ионов СНзСОО и Н сильно понижены. [5]
Ввиду сравнительно слабой диссоциации уксусной кислоты концентрации ионов СНзСОСУ и Н сильно понижены. [6]
Следовательно, слабая диссоциация уксусной кислоты еще в ббльшей степени будет подавлена, и практически концентрация молекул недиссоциированной СН3СООН может быть принята равной общей концентрации кислоты. [7]
Следовательно, слабая диссоциация уксусной кислоты еще в большей степени будет подавлена, и практически концентрация недиссоциированных молекул СН3СООН может быть принята равной общей концентрации кислоты. Так как соль полностью диссоциирует, можно принять общую концентрацию анионов ( не учитывая небольшого их количества, образующегося при диссоциации кислоты) равной общей концентрации соли в буферном растворе. [8]
Следовательно, слабая диссоциация уксусной кислоты еще в большей степени будет подавлена, и практически концентрация недиссоциированных молекул СН3СООН может быть принята равной общей концентрации кислоты. Так как соль полностью диссоциирует, можно принять общую концентрацию анионов ( не учитывая небольшого их количества, образующегося при диссоциации кислоты), равной общей концентрации соли в буферном растворе. [9]
Но ввиду очень слабой диссоциации уксусной кислоты концентрация СНдСООН почти равна заданной концентрации кислоты ck, а ввиду почти полной диссоциаций уксуснокислого натрия почти все СН3СОО - происходят от последнего и равны заданной концентрации соли сс. [10]
Обращает на себя внимание значительно более слабая диссоциация простых алкоголятов по сравнению с полимерными в диметилсульфоксиде, обусловленная, как можно предположить, участием полимерной цепи в сольватации катиона. [12]
 |
Сравнительная активность ОН-групп при этерификации различными реагентами. [13] |
Все три ОН-группы способны к слабой диссоциации. [14]
Таким образом, можно считать доказанной слабую диссоциацию в кристаллах; но это утверждение потеряет значительную часть своей ценности, если мы вспомним, что диссоциация относится не к самому кристаллу, а только к тем случайным примесям, которые, не имея строго определенного, соответствующего их свойствам места в кристаллической решетке, легко подпадают под действие электрических сил. Снова возникает вопрос: возможна ли частичная тепловая диссоциация ионов самой кристаллической сетки. Нам такое представление кажется вероятным; можно себе представить, что некоторые ионы удаляются из своего положения равновесия настолько, что электромагнитное поле в кристалле не имеет более тенденции вернуть их в прежнее положение; такой ион получает возможность двигаться между элементами кристаллической решетки, либо сохраняя свою индивидуальность, либо же замещая по пути один из однозначных с ним ионов сетки, который сам переходит на положение странствующего свободного иона. [15]
Страницы: 1 2 3 4