Инверсия - сахароза
Cтраница 1
Инверсия сахарозы в загрязненных сахарных растворах протекает значительно слабее, чем в чистых растворах сахарозы. Загрязненные сахарные растворы обладают буферными свойствами по отношению к каталитическому действию Н - ионов. [1]
Инверсия сахарозы кислотами является специфическим катализом ионами водорода. Скорость реакции пропорциональна концентрации водородных ионов. Вероятный механизм инверсии сахарозы и всех реакций гидролиза олигосахаридов и гликозидов следующий: в первой фазе присоединяется ион водорода к атому кислорода окисного мостика. Далее продукт присоединения взаимодействует бимо-лекулярно с водой, регенерируя протон. [2]
Инверсия сахарозы легко проходит при действии разбавленных минеральных кислот и скорость инверсии может служить мерилом силы кислот. [3]
Инверсии сахарозы способствует также повышение температуры раствора. [4]
Инверсия сахарозы легко проходит при действии разбавленных минеральных кислот и скорость инверсии может служить мерилом силы кислот. [5]
Инверсия сахарозы, катализируемая ферментом р-фруктофуранозидазой ( инвертазой), использована для определения ( 1 - 5) 10 - 7 М ионов серебра, которые являются ингибиторами реакции, так как образуют с инвертазой устойчивый неактивный комплекс. Определение проводят при рН 5 5, скорость реакции измеряют поляриметрическим методом. [6]
Скорость инверсии сахарозы катионитом зависит от скорости диффузии сахарозы внутрь зерна и скорости диффузии инвертного сахара из зерна. [7]
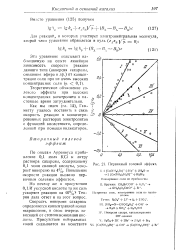 |
Первичный солевой аффект. [8] |
Скорость инверсии сахарозы определяется концентрацией ионов гидроксония, в свою очередь зависящей от степени ионизации кислоты. [9]
Кинотика инверсии сахарозы и присутствии понтон. [10]
Гидролиз или инверсия сахарозы и гидролиз сложных эфиров принадлежат к кислотно-каталитическим реакциям, которые были изучены первыми. Оствальд [5] суммировал данные по скорости гидролиза метилацетата и сахарозы в нормальных растворах кислот и показал, что скорость, отнесенная к скорости в растворе нормальной соляной кислоты ( с такой же концентрацией реагирующего вещества), полностью соответствует изменениям относительной электропроводности кислот. Оствальд и Аррениус считали, что электропроводность меняется с глубиной диссоциации кислоты согласно константе диссоциации и что соответствие в поведении показывает, что скорости, по-видимому, изменяются с концентрацией водородных ионов, общих для всех этих растворов. [11]
Например, инверсия сахарозы в присутствии ионов Н в качестве катализатора в целом есть реакция третьего порядка. [12]
В результате инверсии сахарозы образуется оптически деятельный инвертный сахар. Если вся сахароза проинвертирует, то концентрация образовавшегося инвертного сахара будет пропорциональна концентрации взятой навеске сахарозы в начальный момент. [13]
Наблюдение за инверсией сахарозы рекомендуется вести с помощью поляриметра. [14]
С целью снижения инверсии сахарозы при фильтрации сахарных растворов через катионит в Н - форме следует поддерживать минимально возможную температуру фильтруемых растворов. [15]
Страницы: 1 2 3 4