Полная диссоциация
Cтраница 1
Полная диссоциация достигается лишь тогда, когда значение рН становится немного ниже той точки, при которой наступает растворение кремнезема, и то только в присутствии раствора сильной соли ( см. гл. [1]
Полная диссоциация эфиратов весьма затруднена. Эфир можно вытеснить более основным растворителем, таким, как тетрагидро-фуран или пиридин, с дальнейшим выделением тепла; последнее обстоятельство указывает на то, что эти растворители соединены еще прочнее. Устойчивость подобных сольватов резко отличается от устойчивости сольватов диалкилмагния, диссоциирующих при слабом нагревании ( стр. [2]
Полной Диссоциации нет, но взаимодействие R и Hal ослаблено. [3]
Полной диссоциации нет, но взаимодействие R и Hal ослаблено. [4]
О полной диссоциации на металл и 02 в условиях окислительного катализа не может быть и речи. [5]
При полной диссоциации свободная фосфорновольфрамовая кислота должна была бы обнаружить более высокую электропроводность. [6]
Константа полной диссоциации К равна произведению констант диссоциации для отдельных ступеней процесса. [7]
При полной диссоциации а 1 и остается формула для сильных электролитов. [8]
При полной диссоциации в растворе находятся только ионы. [9]
При полной диссоциации одно - одновалентных электролитов с равно молярности с. При неполной диссоциации величину с необходимо заменить произведением са, где с - молярность раствора; а - степень диссоциации. Отметим, кроме того, что D - диэлектрическая проницаемость среды иг ] - вязкость среды при постоянной температуре в разбавленном растворе являются величинами постоянными. [10]
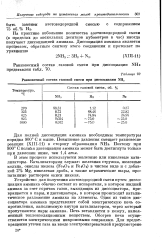 |
Равновесный состав газовой смеси при диссоциации NH3. [11] |
Для полной диссоциации аммиака необходимы температуры порядка 900 С и выше. Повышение давления смещает равновесие реакции ( XIII-H) в сторону образования NHs. Поэтому при 900 С полная диссоциация аммиака может быть достигнута только при давлении ниже, чем 1 4 атм. [12]
Допустимость полной диссоциации солей в морской воде, например, приводила к выводу о пересыщении этой воды по карбонату кальция, в то время как фактически этого не было. [13]
Константа полной диссоциации электролита равна произведению констант его диссоциации по ступеням. [14]
Теория полной диссоциации сильных электролитов требует, чтобы свойства разбавленных растворов этих электролитов полностью определялись отдельными ионами; так, свойства разбавленного раствора соляной кислоты должны определяться свойствами ионов водорода и ионов хлора. Особый интерес представляют в данном случае термохимические свойства. [15]
Страницы: 1 2 3 4