Полная диссоциация
Cтраница 4
Для многих электролитов полная диссоциация имеет место даже при больших концентрациях; это так называемые сильные электролиты. К ним указанное соотношение между степенью диссоциации и электропроводностью неприменимо. Для других же электролитов даже при очень большом разбавлении степень диссоциации остается значительно меньше единицы. [46]
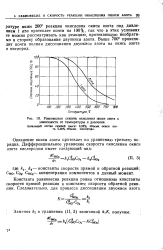 |
Равновесная степень окисления окиси азота в зависимости от температуры и давления. [47] |
Выше 700 происходит почти полная диссоциация двуокиси азота на окись азота и кислород. [48]
Хорошо известным примером полной диссоциации могут служить АИ - в 1 соединения. Он пришел к заключению, что кинетика процесса включает диффузию поверхностных атомов А я В с последующей рекомбинацией атомов В и образованием молекул flj до перехода в газообразную фазу. [49]
Следовательно, при полной диссоциации 0 05 г-моля гидроокиси калия образуется 0 05 г-иона гидроксила. [50]
Константы нестойкости при полной диссоциации тех же ионов равны: 7 8 - 10 - 6 и 7ЫО-36. [51]
При полной или почти полной диссоциации состояние протона совершенно не зависит, от какого аниона он отщепился. [52]
Сделанное допущение о полной диссоциации сильных электролитов в растворе имеет ряд убедительных доказательств. [53]
 |
Зависимость интегральной эн - ДН тальпии растворения КС1 от разбавления. [54] |
Этот факт подтверждает полную диссоциацию сильных электролитов в разбавленных водных растворах. [55]
Данные распределения подтверждают практически полную диссоциацию хлористого лития в изоамиловом спирте. [56]
Заметим здесь, что полная диссоциация кислоты - удаление разорвавшегося-иона гидриксония за пределы притяжения его ионным остатком - фиктивный процесс; удаляется на ион гидроксония, а протон, при - этом необязательно тот протон, который отщепился от молекулы кислоты и который мы отметили на приведенной выше схеме звездочкой. Процесс диссоциации кислот, в отличие от процесса диссоциации солей, напоминает, таким образом, бег с эстафетой. [57]
Страницы: 1 2 3 4