Полная диссоциация
Cтраница 3
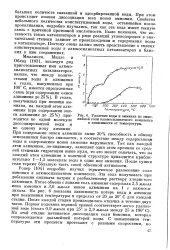 |
Удаление воды и аммиака из аммонийной соли алюмосиликатного комплекса в зависимости от температуры. [31] |
При этом-происходит полная диссоциация всех ионов аммония. Свойства небольшого количества конституционной воды, остающейся после-прокаливания, подробно изучались, так как эта вода имеет тесную связь с причиной протонной кислотности. Было показано, что активность таких катализаторов в ряде реакций углеводородов в значительной степени зависит от происхождения и содержания воды в катализаторе. Поэтому очень важно иметь представление о связях конституционной воды в алюмосиликатных катализаторах и близких к ним соединениях. [32]
С происходит почти полная диссоциация NOa на окись азота и кислород. [33]
Для случая полной диссоциации величина i, согласно классической теории, будет равняться числу ионов, на которое распадается каждая внесенная в раствор молекула. [34]
Для случая полной диссоциации величина i, согласно классической теории, будет равняться числу ионов, на которое распадается каждая внесенная в раствор молекула. [35]
Поскольку при полной диссоциации t 0, в любой момент времени J равняется нулю. [36]
В условиях полной диссоциации обеих функциональных групп такого рода ионит в некоторых случаях должен вести себя, по-видимому, подобно бифункциональному иониту, содержащему функциональные группы различной природы. [37]
Для случая полной диссоциации величина i, согласно классической теории, будет равняться числу ионов, на которое распадается каждая внесенная в раствор молекула. [38]
В случае полной диссоциации электролита, при наличии достаточно точных данных по зависимости интегральных теплот растворения от концентрации и концентрационной зависимости давлений насыщенных паров растворителя над растворами, AS может быть вычислена с вполне удовлетворительной точностью. В средах со средними и, особенно, низкими значениями диэлектрической проницаемости возникают затруднения, связанные с невозможностью одновременной надежной оценки степени диссоциации ( а) и активности. [39]
В случае полной диссоциации электролита, при наличии достаточно точных данных по зависимости интегральных теплот растворения от концентрации и концентрационной зависимости давлении насыщенных паров растворителя над растворами, ASf может быть вычислена с вполне удовлетворительной точностью. В средах со средними и, особенно, низкими значениями диэлектрической проницаемости возникают затруднения, связанные с невозможностью одновременной надежной оценки степени диссоциации ( а. [40]
 |
Зависимость эквивалентной электролроводности от Ус для разбавленных рас. - творов сильных электролитов. [41] |
Учитывая, полную диссоциацию с и л ь н ы х электролитов в растворах различных концентраций, на первый взгляд можно было бы ожидать, что Kv таких растворов должна быть равной АО. Этого, однако, не происходит, так как по мере повышения концентрации ионов в растворе средние расстояния между ними уменьшаются, что приводит к возрастанию их взаимного притяжения. В результате перемещение каждого иона по объему раствора затрудняется и с повышением концентрации эквивалентная электропроводность К уменьшается. [42]
Несмотря на полную диссоциацию сильных электролитов, их электропроводность с ростом концентрации раствора уменьшается. Теоретическое обсуждение этого явления, предпринятое Дебаем, Гюккелем и Онзагером, исходит из того факта, что при наложении внешнего электрического поля, помимо поступательного движения ионов к электродам, осложняемого их тепловым движением, необходимо учесть силы трения сольватированных ионов о растворитель и тормозящий эффект, возникающий вследствие электростатического взаимодействия ионов между собой. [43]
Несмотря на полную диссоциацию сильных электролитов, их электропроводность с ростом концентрации раствора уменьшается. [44]
Несмотря на полную диссоциацию сильных электролитов, их электропроводность с ростом концентрации раствора уменьшается. При теоретическом обосновании этого явления Дебай, Хкжкель и Онзагер исходили из того, что при наложении внешнего электрического поля, помимо поступательного движения ионов к электродам, осложняемого их тепловым движением, необходимо учитывать силы трения сольватированных ионов о растворитель, а также тормозящий эффект, возникающий вследствие электростатического взаимодействия ионов. [45]
Страницы: 1 2 3 4