Ингибирование - холинэстераза
Cтраница 3
Хотя степень ингибирования холинэстеразы сильно меняется, но она компенсируется тем успехом, который достигается при применении этих сильных ингибиторов. Херменц и Гудвин [79] и Рейделев и Вудард [ 160а ] приводят данные о нормальной активности холинэстеразы эритроцитов коровы. Снижение количества холинэстеразы эритроцитов еще не является неблагоприятной реакцией, так как подобная депрессия может быть вызвана ( а может и не быть) уменьшением количества этих ферментов в жизненно важных тканях. [31]
Отсюда был сделан принципиальной важности вывод о том, что в основе механизма ингибирования холинэстераз фос-форорганическими соединениями лежит необратимая химическая реакция бимолекулярного механизма. При этом оказалось, что бимолекулярные константы скорости ингибирования холинэстераз имеют, как правило, очень большие величины. [32]
Изучение механизма действия фосфорорганических инсектицидов и акарицидов по отношению к млекопитающим и членистоногим показало, что в организме животных они фосфорили-руют жизненно важные ферменты - эстеразы, подавляя их нормальные функции. Полагают [2], что действие этих соединений заключается главным образом в ингибировании холинэстеразы. Фосфорорганические соединения связывают холинэстеразу ( схема 2), в результате она теряет свою активность и не может вызывать гидролиз ацетилхолина. [33]
Безопасный срок работы определяется начальной концентрацией пестицидов на растениях. Путем комплексного исследования смывов с листьев, рук рабочих и экспозиционных тестов ингибирования холинэстеразы определен безопасный срок начала работы после обработки растений фосфорор-ганическими пестицидами. Предложены номограммы для практического использования. [34]
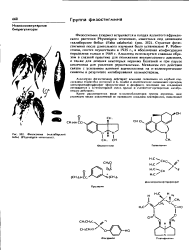 |
Фиюстигма ( калабарский боб ( Physosligma venenosum. [35] |
Робинсоном, синтез осуществлен в 1935 г., а абсолютная конфигурация определена только в 1969 г. Алкалоид используется главным образом в глазной практике для понижения внутриглазного давления, а также для лечения некоторых нервных болезней и при парезе кишечника для усиления перистальтики. Механизм его действия связан с усилением влияния ацетилхолина на н-холинергические синапсы в результате ингибирования холинэстеразы. [36]
В 1940 г. был обнаружен факт чрезвычайной токсичности диалкилмонофторфосфатов. В последующие годы было установлено, что токсичность диметилового эфира является результатом эффекта ингибирования холинэстеразы, вследствие чего происходит быстрое накопление ацетилхолина, выделяющегося при нервных импульсах. Диксон и Нидхэм установили, что ДФП является одним из наиболее специфичных и сильных из известных в настоящее время ингибиторов ферментов. Они наблюдали, что токсическое действие этого вещества при вдыхании его паров животными выше соответствующего действия фосгена, хлор-циана, хлорпикрина и сравнимо с токсическим действием синильной кислоты. Кильбай и Кильбай наблюдали сильное действие этого вещества на человеческий организм; по их описаниям, это действие аналогично описанному Ланге и Крюгером; в процессе опытов два человека подвергались действию ДФП в течение 3 мин. При действии ДФП на животных в несколько более высокой концентрации в течение 10 мин. [37]
 |
Топография гидрофобных участков активной поверхности АХЭ и БуХЭ. [38] |
Молекулы спирта, адсорбируясь на гидрофобных участках белка, должны ослаблять гидрофобное взаимодействие, и константа скорости ингибирования холинэстераз незаряженными ФОИ с объемистыми углеводородными радикалами должна понижаться. [39]
Дальнейшие исследования, проведенные в Институте нефтехимического синтеза им. Было показано, что у VI ( R - R - алкокси, Х - трихлоралкокси) увеличение длины алкильных цепочек в R и R от Q до С4, в соответствии с общими закономерностями [91], уменьшает антихолинэстеразную активность, а переход от соединений нормального ряда к изо-алкоксипроизводным усиливает ингибирование холинэстеразы. [40]
Для определения остаточных количеств фосфорорганических инсектицидов и карбаматов авторы работы [146] использовали систему ВЭЖХ в сочетании с автоматическим анализатором ингибиторов холинэстеразы. В большинстве случаев эти пределы удовлетворяют требованиям анализа остатков; причем следует отметить, что содержащиеся в экстракте другие ингибиторы холинэстеразы определению не мешают. Метод ингибирования холинэстеразы имеет еще одно преимущество по сравнению с другими методами определения остаточных количеств карбаматов: предварительный гидролиз и ( или) получение производных в данном случае не нужны. [41]
Как бы то ни было, яды Таммелипа оказались в десятки раз более токсичными, чем даже такое сильнодействующее ФОС, как зарин. Образовавшаяся фосфорилированная холинэстераза в отличие от ацетили-рованной является соединением достаточно прочным и не подвергается самопроизвольному гидролизу. Оказалось, что процесс ингибирования холинэстеразы является двухэтапным. Оба эти этапа являются результатом сложной, до конца еще не выясненной молекулярной перестройки в комплексе ФОС-холинэстераза. Забегая несколько вперед, отметим значимость данного явления для практики применения некоторых антидотов, действие которых заключается в разрыве химической связи между ядом и ферментом. Таким образом, под влиянием антихолинэсте-разных веществ тормозится разрушение молекул ацз-тилхолина и он продолжает оказывать непрерывное действие на холинорецепторы. [42]
Автоматизированный метод особенно удобен для исследования кинетики взаимодействия холинзстераз с ингибиторами, протекающего часто с такой высокой скоростью, что ее измерения вручную неэффективны. Проводя реакцию в отсутствие ингибитора ( рис. 41, прямая 1) и в его присутствии ( рис. 41, кривая 2), можно получить на ленте самописца кинетические кривые, обработка которых указанным в гл. ИЗ) позволяет рассчитать константу скорости ингибирования холинэстеразы. [43]
Гидрофобные взаимодействия, как было показано в работах нашего коллектива [1], играют существенную роль при реакциях фосфорорганических соединений ( ФОС) с холинэстеразами. Эти взаимодействия очень четко проявляются в ряду 0 8-диалкилметилтиофосфонатов. Представляет интерес выяснить значение указанных взаимодействий при ингибировании холинэстераз с помощью ФОС более сложного строения, например содержащих в 3-положении тиоэфирного остатка какие-либо дипольные группировки. Особенно важным здесь является выявление различий в реакциях ФОС с холинэстеразами разных типов. [44]
Приме нение таких соединений в сельском хозяйстве вполне безопасно. Изучение механизма действия органических соединений фосфора на млекопитающих и насекомых показало, что в организме животных они фосфорилируют жизненно важные эстеразы, инги-бируя их нормальные функции. Полагают, что действие этих соединений направляется главным образом на ингибирование холинэстеразы, физиологические функции которой в организме животных очень важны. [45]
Страницы: 1 2 3 4