Азирин
Cтраница 1
Азирин 549 производные получение 32, 319, 364, 547, 550 реакции 22, 35, 316, 344, 547, 550, 553 ел. [1]
 |
Электроциклнческне реакции с участием четырех - или шестн-т-электрон-ных линейных изомеров. [2] |
Образование азиринов при фотохимическом разложении винила-зидов ( пример 4) можно рассматривать как внутримолекулярное присоединение нитрена к двойной связи. [3]
В отличие от азиринов трехчленные циклические азометины, содержащие два гетероатома [ диазирины ( 3046), оксазирины ( 304в) и тиазирины ( 304г), неизвестны. Предполагают, что диазирины и тиазирины могут участвовать как неустойчивые промежуточные соединения в фотохимически индуцированных реакциях 1 3-дипо-лярного циклоприсоедчнения, в которые вступают некоторые ме-зоионные гетероциклы. Так, возможно, что образование производных пиразола ( 327а) и изотиазола ( 3276) при фотолизе сиднонов ( 324а) и их тиаанологов ( 3246) в присутствии диметилового эфира ацетйлендикарбоновой кислоты ( ДМАД) происходит по уравнению ПО. [4]
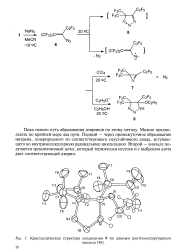 |
Кристаллическая структура соединения 9 по данным рентгеноструктурного. [5] |
Пока неясен путь образования азиринов по этому методу. [6]
Реакционная способность двойной связи азиринов отражается в легкости ее участия как 2я - компонента в реакциях типа присоединения по Дильсу-Альдеру и ( в меньшей степени) в реакциях 1 3-диполярного циклоприсоединения. [7]
Низкая основность А - азиринов объясняется тем, что орбиталь у атома азота, содержащего неподеленную электронную пару, приобрела в значительной мере s - характер. Раскрытие цикла азиридиновых интермедиатов ( 345; R3 H), образующихся при гидратации азиринов ( 343), представляет собой удобный способ получения ос-аминокетоноа ( 348) [233], который аналогичен перегруппировке Небера ( см. с. Таким образом, синтез а-аминокетонов путем сольволиза азиринов часто дополняет перегруппировку Небера, поскольку можно получать изомерные а-аминокетоны. Сольволиз азиринов можно использовать и для получения а-аминоальдегидов ( например, если применять 2-незамещенные азирины), которые невозможно получить посредством перегруппировки Небера, так как тозилаты альдок-симов превращаются главным образом в нитрилы. [8]
Реакционная способность А - азиринов по отношению к нуклео-фильным реагентам по своему характеру сходна с той, которую они проявляют в реакциях с электрофильными агентами. [9]
Реакционная способность двойной связи азиринов отражается в легкости ее участия как 2л - компонента в реакциях типа присоединения по Дильсу-Альдеру и ( в меньшей степени) в реакциях 1 3-диполярного циклоприсоединения. [10]
Из двух возможных изомеров азирина только 2Н - азирин был выделен и охарактеризован. Родоначальник класса - соединение 9 ( R1, R2, R3 Н) был получен, но оказался неустойчивым при температуре выше температуры жидкого азота. Многие другие 2Н - ази-рины могут быть выделены и представляют собой жидкости или низкоплавкие твердые вещества. Доказательством циклического напряжения в 2Н - азиринах служит аномально высокая частота колебания группы С N в ИК-спект-рах и КССВ 13С - Н в спектрах ЯМР ( см. гл. [11]
Первый общий синтез 2Я - азиринов был развит Смолинским [ Юа ] и использовал парофазный пиролиз а-винилазидов. [12]
Получен широкий ряд 2Я - азиринов, включающий конденсированную бициклическую систему ( 11) [3, 13]; выходы в целом хорошие и побочных продуктов образуется немного. [13]
Катализируемый кислотой гидролиз 2Я - азиринов, получаемых фотолизом винилазидов, с образованием а-аминокетонов является полезным дополнением к реакции Небера схема ( 5), поскольку позволяет получать аминокетоны, например ( 19) схема ( 6), которые не всегда доступны с помощью реакции Небера. [14]
Первый общий синтез 2Я - азиринов был развит Смолинским [ Юа ] и использовал парофазный пиролиз ос-винилазидов. Юб ] дают при пиролизе продукты, отличающиеся от 2Я - азиринов. [15]
Страницы: 1 2 3 4