Время - жизнь - радикал
Cтраница 1
Время жизни радикалов с числом атомов углерода больше трех при атмосферном давлении значительно меньше указанной выше величины. Бутильный и пропильный радикалы нестойки и разлагаются, образуя радикалы метил и этил. [1]
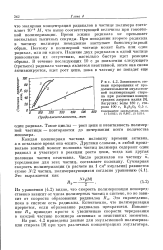 |
Зависимость степени превращения от продолжительности эмульсионной полимеризации стирола при различных концентрациях лаурата калия. Загрузка. воды 180 г, стирола 100 г, K2S2OS 0 5 г. [2] |
Время жизни радикала не превышает нескольких тысячных секунды. При попадании второго радикала в частицу полимера немедленно наступает бимолекулярный обрыв. Поэтому в полимерной частице может быть или один радикал, или ни одного. Наличие двух радикалов в одной частице равнозначно их отсутствию, настолько быстро идет реакция обрыва. [3]
Время жизни радикалов может быть увеличено за счет механических препятствий протеканию бимолекулярных реакций. [4]
Время жизни радикала в водном растворе невелико, и радикальные реакции происходят только в особых условиях. Наряду с этим в воде, молекулы которой связаны водородными связями, при обычной температуре диссоциация на Н и ОН - незначительна, и обмен Н с Н2О и с ОН - очень быстрый. [5]
Время жизни радикалов увеличн - тся при их мезомерноЙ стабилизации. [6]
Времена жизни радикалов и других промежуточных частиц достаточно велики, так что в результате диффузии создаются одинаковые концентрации по всему объему. [7]
Время жизни радикалов R составляет 10 - 8 сек ( в полиэтилене), а для ROO эта величина возрастает до 10 - 2 сек. [8]
Оценено время жизни слабо связанного радикала при 150 С, значение которого оказалось равным около 10 - 6 сек. [9]
Увеличению времени жизни радикалов способствует глубокое охлаждение полученных радикалов ( закалка), а также увеличение диаметра сосуда. [10]
 |
Зависимость скоростей расходования и образования веществ при окислительной полимеризации метилметакрилаталт давления кислорода. [11] |
Па, возрастает время жизни радикала - М - и соответственно увеличивается доля реакций ( 3), скорость расходования мономера и число звеньев - ММ - в цепях полимерной перекиси. [12]
Тем не менее время жизни радикала метила меньше миллисекунды в зависимости от молекул, которые он встречает на своем пути. [13]
С понижением / oz растет время жизни стирольных радикалов и поэтому увеличивается скорость перегруппировки и деполимеризации радикала с образованием неперекисных продуктов. Окись стирола и бензальдегид образуются цепным путем. [14]
С понижением / о2 растет время жизни стирольных радикалов и поэтому увеличивается скорость перегруппировки и деполимеризации радикала с образованием неперекисных продуктов. Эти реакции с уменьшением / о2 все сильнее вытесняют реакцию образования перекиси, но общая скорость реакции меняется незначительно до рог 10 мм рт. ст. Окись стирола и бензальдегид образуюгся ценным путем. С увеличением ро2 растет относительное содержание таких радикалов, и максимум выхода альдегидов достигается при больших рог. [15]
Страницы: 1 2 3 4