Энергия - диссоциация - двухатомная молекула
Cтраница 1
Энергия диссоциации двухатомной молекулы равна энергии связи между атомами в этой молекуле. [1]
Энергии диссоциации двухатомных молекул определяются на основании данных анализа молекулярных спектров. [2]
Энергии диссоциации двухатомных молекул часто могут быть измерены и использованы для вычисления теплот других реакций. [3]
Энергии диссоциации двухатомных молекул закономерно зависят от природы химической связи. При одинаковых анионах замена металлов а-подгрупп их - аналогами также приводит к уменьшению D. Вместе с тем, изменение валентности металлов мало влияет на энергию диссоциации двухатомных молекул. Количественная интерпретация этого факта будет дана в дальнейшем изложении, а пока остановимся на качественной стороне явления. [4]
Энергии диссоциации двухатомных молекул определяются на основании данных анализа молекулярных спектров. [5]
Энергия диссоциации двухатомных молекул равна 1 78 эв и теплота испарения - 95 4 ккал / молъ. [6]
Энергия диссоциации двухатомной молекулы равна энергии связи двух атомов. [7]
Для энергии диссоциации двухатомной молекулы XY сохраняется то же определение. Продуктами процесса диссоциации являются атомы X и Y в своих основных состояниях. [8]
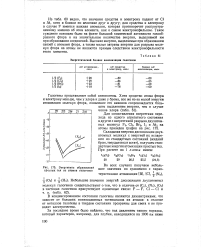 |
Энергетический баланс анионизации галогенов.| Энергетика образования простых тел из атомов галогенов. [9] |
Складывая энергию диссоциации двухатомных молекул с энергией их испарения из стандартных состояний ( жидкий бром, твердые иод и астат), получаем стандартные энергии атомизации простых тел. [10]
В ряде случаев энергия диссоциации двухатомной молекулы может быть определена из анализа предиссоциации в ее спектре. Если спектр обрывается ( или размывается) в результате предиссоциации на отдельных вращательных линиях в нескольких полосах данной системы полос, экстраполяция к границе диссоциации может быть проведена с высокой точностью. [11]
На акую величину отличается энергия диссоциации двухатомной молекулы DO определяемая экспериментально, от энергии диссоциации De, отсчитываемой от минимума кривой потенциальной энергии. [12]
В таблице приведены значения энергий диссоциации двухатомных молекул. Расположение выдержано в алфавитном порядке. [13]
В табл. 1 приведены значения энергий диссоциации двухатомных молекул. Расположение молекул выдержано в алфавитном порядке. Однако соединения металлов с металлоидами помещены на место соединений данного металла. В соответствии с этим CuBr идет после Gu2, а не после BrCl, также как ZnGl после ZnBr, а не после СЮ. [14]
По сравнению с задачей расчета энергий диссоциации двухатомных молекул теоретическое исследование связи в твердых телах с помощью кванто-во-механических принципов оказывается значительно более трудным - В принципе можно написать выражение для энергии сцепления [8] через посредство атомных волновых функций, но до настоящего времени результаты, имеющие термохимическую значимость, не были получены. [15]
Страницы: 1 2 3 4