Выделение - кобальт
Cтраница 2
Гуинн и Хорн [8] предложили применять в качестве носителя для термической декобальтизации активированный уголь, который после определенного насыщения сжигается для выделения кобальта. Образующаяся окись кобальта в дальнейшем, очевидно, переводится в соль жирной кислоты. [16]
Можно предположить, что Со ( П) способен образовывать с одним и тем же тиолом несколько комплексов различного состава [732], некоторые из которых настолько прочны, что почти не вступают в электрохимическую реакцию с выделением кобальта, а вызывают лишь каталитическое выделение водорода. [17]
Электрохимические методы разделения применяются не так часто. Выделение кобальта электролизом из аммиачных растворов позволяет отделять его от цинка, кадмия и других элементов, однако медь и никель также осаждаются на катоде. [18]
Очень удобно применять этот метод к фильтратам, получающимся при отделении пиридином подгруппы железа от двухвалентных металлов третьей аналитической группы, щелочных земель, магния и щелочей. Для выделения кобальта и никеля фильтрат нагревают, добавляют раствор соли пиридина и обрабатывают сероводородом. [19]
Очень удобно применять этот метод к фильтратам, получающимся при отделении пиридином подгруппы железа от двухвалентных металлов третьей аналитической группы, магния, щелочноземельных и щелочных металлов. Для выделения кобальта и никеля фильтрат нагревают, добавляют раствор соли пиридина и обрабатывают сероводородом. [20]
 |
Диффузионный профиль границы раздела эмаль-железо после нагрева при 950 С в течение 10 мин. [21] |
Источниками возникновения микроэлементов служат: микронеоднородность исходной поверхности и расплава эмали, а также выделяющиеся в процессе окислительно-восстановительных реакций частицы Со, Ni на границе раздела. Вследствие выделения кобальта как более электроположительного металла на поверхности стали создается множество микрогальванических пар, усиливающих протекание реакций на границе раздела и разрыхляющих поверхность, что обеспечивает хорошее сцепление. [22]
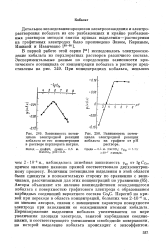 |
Зависимость потенциала электродной реакции.| Зависимость потенциала электродной реакции кобальта от его концентрации кобальта на графите от рН. [23] |
Перенапряжение выделения кобальта увеличивается по мере увеличения площади электрода, занятой карбидными соединениями, и соответствующего уменьшения свободной поверхности, на которой выделение кобальта происходит с экзоэффектом. [24]
В этих случаях приведенный выше метод непригоден. При выделении кобальта купралем одновременно выделяется весь никель в виде объемистого осадка, с трудом экстрагируемого даже большим объемом этилацетата. Кроме того, описанный выше метод вытеснения дитиокарбамата никеля из органического растворителя цианидом калия или хлоридом ртути ( II) является количественным только при отделении малых количеств ( миллиграммов) никеля. Поэтому был выбран другой путь, подробно описанный ниже. В аммиачной среде комплексонатов никеля и кобальта количественно вытесняется ионами кальция только кобальт, а никель выделяется только в незначительной степени. [25]
В этих случаях приведенный выше метод непригоден. При выделении кобальта купралем одновременно выделяется весь никель в виде объемистого осадка, с трудом экстрагируемого даже большим количеством этилацетата. Кроме того, описанный выше метод вытеснения дитиокарбамата никеля из органического растворителя цианидом калия или хлоридом ртути ( II) является количественным только при отделении кобальта от малых количеств ( миллиграммов) никеля. Поэтому был выбран другой метод, подробно описанный ниже. В аммиачной среде комплексонатов никеля и кобальта количественно вытесняется ионами кальция только кобальт, а никель выделяется лишь в незначительной степени. [26]
Ионообменные смолы пока не нашли применения для извлечения кобальта из растворов, однако с этой целью проводятся многочисленные исследования. Часть из них посвящена хрома-тографическому выделению кобальта и его отделению от других компонентов. [27]
Как отмечалось выше, чистый кобальт производят электролитическим рафинированием металла, полученного термическим восстановлением оксида кобальта, который содержит значительные примеси никеля, железа и других металлов. Благодаря высокой катодной поляризации при выделении кобальта становится возможным включение в катодный осадок не только меди, но и никеля, и железа. Поэтому для получения1 чистого кобальта4 требуется весьма тщательная очистка ряетвора от этих примесей, особенно от никеля. [28]
Как отмечалось выше, чистый кобальт производят электролитическим рафинированием металла, полученного термическим восстановлением оксида кобальта, который содержит значительные примеси никеля, железа и других металлов. Благодаря высокой катодной поляризации при выделении кобальта становится возможным включение в катодный осадок не только меди, но и-никеля, и железа. Поэтому для получения чистого кобальт требуется весьма тщательная очистка раствора от этих примесей, особенно от никеля. [29]
Благодаря высокой катодной поляризации при выделении кобальта становится возможным включение в катодный осадок не только меди, но и никеля, и железа. Поэтому для получения чистого кобальта требуется весьма тщательная очистка раствора от этих примесей, особенно от никеля. [30]
Страницы: 1 2 3 4