Выделение - кобальт
Cтраница 3
Совместное восстановление ионов никеля и кобальта [63, 64] является примером такой сопряженной системы. Как видно из рисунка, потенциалы выделения кобальта намного положительней, чем потенциалы выделения никеля, несмотря на то что стандартный потенциал кобальта примерно на 20 мв отрицательнее стандартного потенциала никеля. Это связано с тем, что никель выделяется со значительно большим перенапряжением, чем кобальт. Поляризационная кривая совместного разряда ионов никеля и кобальта находится между кривыми, полученными при раздельном восстановлении этих металлов. [31]
Соловьевой и О. А. Абрарова отрицается роль адсорбированного водорода в явлениях электроосаждения металлов на том основании, что авторами не обнаружено простого параллелизма между выходом по току водорода и величиной перенапряжения металла. Кроме того, высокая поляризация при выделении кобальта наблюдалась ими и тогда, когда, по их мнению, весь ток расходуется на разряд ионов кобальта. Следует, однако, иметь в виду, что доля тока, идущая на выделение водорода, не определяет непосредственно количества водорода, адсорбированного поверхностью металла. Последнее зависит, прежде всего, от природы и потенциала электрода. Известно, что кобальт и никель обладают высокой адсорбционной способностью по отношению к водороду. Этого количества водорода вполне достаточно для создания и сохранения поверхностной пленки, затрудняющей разряд ионов кобальта. Рассмотренное ранее влияние анионов и катионов накладывается на тормозящее действие адсорбированного водорода и приводят к соответствующим изменениям потенциала электрода. [32]
 |
Влияние типа раствора и значения рН на скорость осаждения и сплава Со - Р. [33] |
Реакция химического восстановления ионов кобальта до металла наиболее благоприятно протекает в щелочной среде с использованием в качестве восстановителя преимущественно гипофосфита или борана натрия. В последнее время появились сообщения о возможности выделения кобальта из слабокислых растворов в присутствии восстановителя - диметиламиноборана [ 85, с. [34]
Перенапряжение при выделении некоторых металлов настолько велико, что разности потенциалов между цементируемым и цементирующим металлами не хватает для разряда цементируемого иона, например, кобальт не цементируется цинком из водных растворов на холоду. Замена электролита на такой, в котором перенапряжение выделения кобальта меньше, а потенциал цинка более электроотрицателен вследствие комплексообразо-вания, например, проведение цементации в аммиачной среде, дает возможность процементировать кобальт с достаточной скоростью. [35]
Очистка от кобальта является наиболее ответственной стадией, так как по свойствам никель и кобальт весьма сходны. В последнее время наиболее распространен метод гидролиза с выделением кобальта в виде Со ( ОН) 3 после окисления его до Со3 элементарным хлором. Механизм образования Со ( ОН) 3 представлен следующим образом. [36]
В США начинают все больше использовать соли кобальта, которые поступают в реактор растворенными в олефиновом сырье. Вследствие высокой стоимости этих материалов ниже указываются некоторые способы выделения кобальта. [37]
Перенапряжение выделения кобальта увеличивается по мере увеличения площади электрода, занятой карбидными соединениями, и соответствующего уменьшения свободной поверхности, на которой выделение кобальта происходит с экзоэффектом. [38]
Плавка огарка печей КС, получаемого обжигом флотационного никелевого концентрата, отличается возможностью применения более дешевого восстановителя - бессернистого угля или антрацита. Металл, выплавленный из файнштейна, обычно готовый продукт, направляемый потребителю, а полученный из флотационного концентрата подвергают еще и электролизу для дополнительной очистки с выделением кобальта и платиноидов. [39]
Осажденный на стационарном носителе кобальт в стадии образования карбонилов кобальта ( кобальтпзации) смывается с насадки в виде карбонилов и направляется в реакционную зону. Для непрерывного ведения процесса оксосинтеза необходимо иметь не менее двух аппаратов с переключающимися функциями: в то время как в одном происходит карбонилообразование, в другом протекает выделение кобальта из карбонилов. Недостатком этого метода является периодическая работа аппаратов. [40]
Выбор кислоты на стадии разложения карбонилоп определяется легкостью отделения образовавшейся соли от дскобальтизованного продукта. С этой точки зрении рекомендуется применять минеральные или низшие органические кислоты, так как образуемые ими соли кобальта легко переходят из органического растворителя п водный слой, и процесс выделения кобальта из продукта сводится к разделению жидкостей, резко отличающихся но плотности. На этой стадии наиболее удобно получать водорастворимые соли. [41]
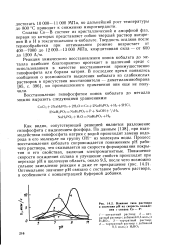
В действительности, суммарная кривая характеризует скорость одновременного протекания трех различных реакций ( восстановления ионов никеля, кобальта и водорода), поэтому на основании этой кривой нельзя определить, как изменяются скорости восстановления ионов металлов при совместном осаждении по сравнению с раздельным осаждением. Для определения изменения указанных скоростей на поляризационных кривых ( 1 - 3) выбрана область потенциалов 550 - 650 мв, в которой определены доли тока, идущие на реакции выделения кобальта, никеля и водорода. Сопоставление скоростей разряда ионов никеля и кобальта при совместном и раздельном восстановлении показывает нарушение закономерностей, вытекающих из теории несопряженных систем. Например, при сравнении скорости выделения никеля без кобальта ( кривая 4) со скоростью выделения никеля совместно с кобальтом ( кривая 6) при 650 мв видно, что скорость разряда ионов никеля при совместном выделении с кобальтом уменьшается примерно в 10 5 раз. Скорость восстановления ионов кобальта совместно с никелем при 550 мв в 16 раз меньше, чем при его раздельном выделении. Следовательно, в данных условиях при совместном осаждении никеля и кобальта происходит торможение скорости восстановления как ионов никеля, так и ионов кобальта. Действительно, в сплавах, полученных при 25 С, содержится преимущественно кобальт. [42]
Отметив недостаточность наших знаний о природе катализирующего процесс действия металлов, авторы [40] сопоставили вероятность инициирования реакции восстановления кобальта медью и платиной. В случае меди, характеризуемой не очень отрицательным потенциалом в кислом растворе кобальтирова-ния ( ф - 0 48 в), отмечается в ряде случаев самопроизвольный скачкообразный сдвиг потенциала в область, соответствующую инициированию выделения кобальта. В случае же платины - металла, который более каталитически активен и характеризуется в этих условиях потенциалом ср; - 0 54 в, инициирования выделения кобальта вообще не происходит. [43]
В этом случае металл осаждают на насадке или на поверхностях нагрева; возможно также удалять его в виде взвеси в продукте реакции или водном слое. Предложен остроумный способ [25], основанный на осаждении кобальта на углеродистой насадке, которую затем сжигают для регенерации металлического кобальта. Для декобальтизации или выделения кобальта из водных растворов предложено [19] использовать ионообменные смолы. [44]
Каждый из этих - сорбентов применяется для выделения следов веществ перед колориметрическим определением. Окись алюминия успешно использовали для выделения кобальта в виде нитрозо - К-комплексной соли ( стр. [45]
Страницы: 1 2 3 4