Выделение - олово
Cтраница 3
Хотя для выделения олова из растворов электролизом предложено, изучено и испытано много способов, но ни один из них не получил широкого применения. Это объясняется как технологическими трудностями, так и экономическими причинами. Пирометаллургия олова при переработке чистых и богатых руд довольно проста. Металл получают достаточной чистоты. Правда, в последнее время приходится перерабатывать и руды, содержащие значительное количество примесей, загрязняющих получаемое олово. Но касситерит SnCb не поддается непосредственному выщелачиванию, и для гидрометаллургической переработки требуется довольно сложная подготовка руды. [31]
В качестве комплексообразователя для ионов олова применяют фториды. Возможно также сближение потенциалов выделения олова и никеля в станнатноцианистом и пирофосфатном электролитах. [32]
Рассчитанные таким образом парциальные плотности тока фиксируются на ординатах точками при каждом значении потенциала, соответствующем плотности тока суммарного процесса. По разнице между потенциалами выделения олова и никеля в сплав и потенциалами раздельного осаждения их при плотности тока 1 - 2 А / дм2 определяют величину деполяризации. [33]
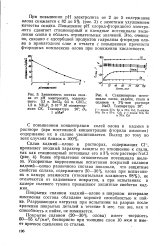
Таким образом, в присутствии фторидов достигается сближение потенциалов олова и никеля и становится возможным совместное осаждение их на катоде. При сопоставлении кривых поляризации выделения олова, никеля и сплава Sn-Mr ( 65 % Sn) при 50 С ( рис. 86) видно, что совместное выделение олова и никеля на катоде происходит при более положительном потенциале, чем выделение олова и никеля в отдельности. [34]
В предыдущей работе было показано [1], что добавление к хлорид-фторидному электролиту 0 5 м / л парафенолсульфоновой кислоты резко повышает катодную поляризацию при электроосаждении олова ( на 0 15 - 0 2 в) и почти не оказывает влияния на поляризацию при выделении никеля. Таким образом, процесс выделения олова значительно тормозится в присутствии парафенолсульфоновой кислоты и поэтому содержание его в сплаве понижается. [35]
 |
Электролитическая ячейка для измерения потенциалов разложения. [36] |
Однако / - F-кривые для системы SnCb - KCI - FeCb, снятые без предварительного электролиза, имеют два излома. Очевидно, соответствующие им потенциалы отвечают выделению олова ( первый потенциал) и затем железа. [37]
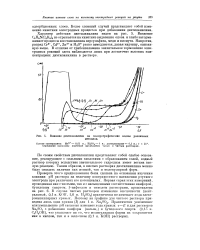
При повышении рН электролита от 2 до 5 содержание олова снижается с 82 до 5 % ( рис. 3) с заметным ухудшением качества осадка. Повышение рН хлорид-фторидного электролита сдвигает стационарный и катодные потенциалы выделения олова в область отрицательных значений. Это, очевидно, связано с адсорбцией продуктов гидролиза фторидов олова в прикатодном слое и отчасти с повышением прочности фторидных комплексов олова при понижении кислотности. [39]
 |
Влияние диэтиланилина на полярографические волны различных. [40] |
Более сложный случай представляет собой изменение кинетики электродных процессов при добавлении диэтиланилина. Введение GeH6N ( G2H5) 3 не отражается на кинетике выделения олова и слабо затормаживает процессы восстановления персульфата, меди и висмута. Напротив, разряд Cr3t, Cd2H, Zn2 и Н30 резко замедляется, давая картину, описанную выше. В отличие от трибензиламина значительное торможение электродных реакций здесь наблюдается лишь при достаточно высоких концентрациях диэтиланилина в растворе. [41]
В работе [17] исследовано полярографическое поведение SnCl2 и FeCl. Деполяризация при выделении железа составляет около 0 2 в, а при выделении олова - около 0 4 в. Она объясняется образованием сплавов на платиновом катоде. [42]
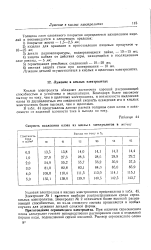 |
Скорость осаждения олова из кислы х электролитов в мк / час. [43] |
Кислые электролиты обладают достаточно хорошей рассеивающей способностью и устойчивы в эксплуатации. Благодаря более высокому выходу по току, чем в щелочных электролитах, и возможности выделения олова из двухвалентных его соединений скорость осаждения его в кислых электролитах более высокая, чем в щелочных. [44]
Из растворов хлористых солей кадмия и олова в отсутствие поверхностноактивных веществ ( ПАВ) на катоде осаждается одно олово. При добавлении к раствору фтористого аммония, который образует комплексные соединения с оловом типа ( NH4) 2SnF4 или ( NH4) 2SnCl2F2, потенциалы выделения олова и кадмия сближаются, но осадки также состоят преимущественно из олова. Исследование влияния большого числа ПАВ катионного характера из группы смачивателей и эмульгаторов, применяющихся в текстильной промышленности, показало, что заметное торможение процесса выделения олова на катоде вызывают алкамон Г и полиэтоксиамин СК. [45]
Страницы: 1 2 3 4