Выход - карбамид
Cтраница 3
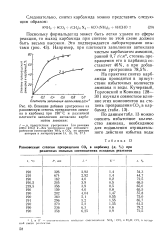
Позднее Кларк, Гедди и Рист [4] определили, что выход карбамида находится в прямолинейной зависимости от обратной величины плотности заполнения реактора. [31]
Поскольку формальдегид может быть легко удален из сферы реакции, то выход карбамида при синтезе по этой схеме должен быть весьма высоким. [33]
Поскольку карбамат аммония наиболее интенсивно превращается в карбамид в жидкой фазе, выход карбамида при лрочих равных условиях возрастает с увеличением степени заполнения реакционного объема, так как чем меньше свободный объем реактора, тем меньшее количество карбамата аммония разлагается с выделением NH3 и СО2 в газовую фазу. [34]
В интервалах давлений и температур, приведенных в таблице, большое влияние на выход карбамида имеет соотношение компонентов реакции. Как следует из таблицы, при указанных выше давлениях и температурах наибольшее значение для увеличения выхода карбамида имеет введение избытка аммиака. [35]
Аммиак связывает воду, удаляя ее из сферы реакции и тем самым способствуя повышению выхода карбамида. С этой целью применяют большой избыток NH3 по отношению к стехиометриче-скому его расходу. С увеличением температуры возрастает также скорость процесса дегидратации карбамата. [36]
Фихтер и Беккер [3] нашли, что при плотности заполнения реактора 0 11 г / см3 выход карбамида с ростом температуры вначале возрастает, достигает максимальной величины при 135 С, а затем уменьшается. Вопрос о наличии максимума на кривых будет подробно рассмотрен при анализе межфазного распределения компонентов. [37]
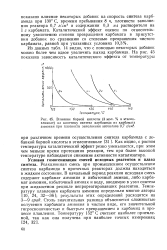 |
Влияние борной кислоты ( 3 мол. % в этилен-гликоле на кинетику синтеза карбамида из карбамата аммония при плотности заполнения автоклава 0 7 г. см3. [38] |
Из данных табл. 14 видно, что с помощью некоторых добавок можно более чем вдвое увеличить выход карбамида. [39]
Под выходом карбамида чаще всего понимают степень превращения в карбамид ( %); возможен подсчет выхода карбамида и по аммиаку. Если в процесс вводят избыток аммиака по отношению к его стехиометрическому количеству, то выход карбамида по аммиаку будет соответственно меньше выхода по двуокиси углерода. [40]
Под выходом карбамида чаще всего понимают степень превращения СО2 в карбамид ( в %); возможен подсчет выхода карбамида и по аммиаку. Если в процесс вводят избыток аммиака по отношению к его стехиометрическому количеству, то выход карбамида по аммиаку будет соответственно меньше выхода по двуокиси углерода. [41]
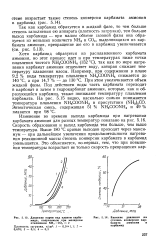 |
Давление паров над плавом карбамида, получаемым при молярном отношении NH3. СО2 2.| Влияние давления на степень конверсии карбамата аммония в карбамид. [42] |
Изменение во времени выхода карбамида при нагревании карбамата аммония для разных температур показано на рис. 5.16. Скорость образования и выход карбамида тем больше, чем выше температура. Выше 180 С кривые выходов проходят через максимум - при дальнейшем увеличении продолжительности нагревания реакционной массы степень конверсии карбамата в карбамид уменьшается. [43]
Влияние температуры на скорость образования карбамида из карбамата аммония показано на рис. 21, на котором приведены кривые изменения выхода карбамида во времени. [44]
Реакция образования карбамата аммония из СО2 и NH3 протекает быстро и практически до конца, реакция же дегидратации карбамата аммония, определяющая выход карбамида, обратима. В соответствии с принципом Ле-Шателье повышение температуры благоприятствует протеканию реакции дегидратации карбамата аммония, однако при этом возможно его разложение. [45]
Страницы: 1 2 3 4 5