Выход - перекись
Cтраница 3
Если допустить, что пероксидирование происходит только согласно уравнениям ( 3) - ( 6), то следует ожидать, что интенсивность предварительного облучения не влияет значительным образом на выход перекисей. Однако интенсивность облучения приобретает большое значение, когда скорость диффузии кислорода в полимере отстает от скорости образования полимерных радикалов. В таком случае в полимере преобладают реакции сшивания и деструкции, однако их можно подавить, увеличив давление кислорода во время облучения. Концентрация полимерных перекисей возрастает с увеличением дозы облучения. Концентрация перекисей в основной цепи полимера определяет количество привитых участков, в то время как их длина регулируется температурой прививки и концентрацией мономера. [31]
Караш, Фоно и Нуденберг12 - получали перекись изопролил-бензола четырьмя различными термическими реакциями, причем наилучшим методом является нагревание 2 моль гидроперекиси изапропилбензола при 95 С с 1 моль диметилфенил-карбинола; выход перекиси изопропилбензола почти количественный. [32]
В нефтяной лаборатории ВТИ разработан ускоренный метод получения этой перекиси окислением тетралина в присутствии катализатора ( 0 01 - 0 002 % нафтената марганца) [199], позволяющий достигнуть того же выхода перекиси в течение 10 - 12 час. Более глубокое окисление ведет к частичному разложению образующейся перекиси, что создает затруднения при последующем ее выделении. При этом выкристаллизовывается перекись в виде бесцветных игл. Полученная сырая перекись ( выход ее 15 - 17 % от окисленного тетралина) отжимается на шоттовском фильтре, промывается 1 - 2 раза холодным петролейным эфиром и дважды перекристаллизовывается из петролейного эфира. Иодометрическое определение активного кислорода подтверждает присутствие одной перекисной группы. [33]
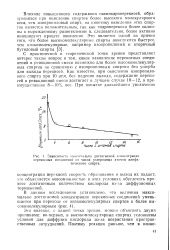 |
Зависимость максимально достигаемой концентрации перекисных соединений от числа углеродных атомов алифатического спирта. [34] |
С практической и теоретической точек зрения представляет интерес также вопрос о том, какое накопление перекисных соединений в реакционной смеси возможно для более высокомолекулярных спиртов по сравнению с изопропиловым спиртом без ущерба для выхода перекисей. Как известно, при окислении изопропило-вого спирта при 10 атм, без падения выхода, содержание перекисей в реакционной смеси достигает в лучшем случае 10 - 12, а преимущественно 8 - 10 % вес. [35]
Как ясно из рис. 36, обработка поверхности реакционного сосуда КС1 почти не оказывает влияния на форму и расположение ( по температуре и давлению) холоднопламенной области ( а также и области самовоспламенения), хотя, как видно из табл. 24, выход перекисей в этом случае равен нулю. Это снова привело Пиза к его первоначальному представлению о незначительной роли органических перекисей в процессе окисления углеводородов. [36]
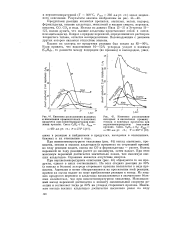
Если рассмотреть с этой точки зрения кинетические кривые перекисных соединений ( рис. 2) и величину выхода перекисей ( рис. 3), то можно констатировать, что максимальный выход перекисей от теории достигается на всем протяжении времени от нуля до imax и относительно выхода перекисей любое время окисления в пределах 0-гтах является благоприятным. [37]
Если рассмотреть с этой точки зрения кинетические кривые перекисных соединений ( рис. 2) и величину выхода перекисей ( рис. 3), то можно констатировать, что максимальный выход перекисей от теории достигается на всем протяжении времени от нуля до тах и относительно выхода перекисей любое время окисления в пределах 0-ттад - является благоприятным. [38]
Влияние различных добавок ( кроме смолы, полностью подавляющей процесс) на скорость реакции сводится к понижению или повышению каталитической активности Н - ионов в реакционной смеси за счет изменения энергии их сольватации в растворе, что так же, как в случае добавок воды, подтверждается практической неизменностью выхода перекиси кумила, несмотря на изменение брутто-скорости реакции. [39]
Когда R является хлором, реакция легко протекает на холоду в эфирном растворе; в этом случае нет необходимости добавлять в систему вещества основного характера. Выход перекиси достигает 61 - 67 %, считая на этил - или грет-бутилгидропере-кись. Лучший выход ( 52 - 94 %) был получен для 1-этоксиизохромана. [40]
Бах [35] нашла, что при автоокислении углеводородов под действием рентгеновских лучей, так же как и при термическом автоокислении, образуются перекиси, карбонильные соединения и кислоты ( концентрации их уменьшаются в приведенной последовательности), но что, за исключением случая циклогексана, в основном образуются диалкилперекиси, а не гидроперекиси, составляющие главную часть при термическом автоокислении или окислении под действием ультрафиолетового света. Выход перекиси не зависит ни от температуры, ни от интенсивности излучения, и поэтому, вероятно, перекиси возникают не в результате цепной реакции. Возможно, что образовавшийся вначале радикал RO2 [ стр. [41]
В отсутствие добавок сильных кислот в изученных условиях в течение длительного времени концентрация исходных веществ совершенно не меняется. Выход перекиси кумила во всех нижеописанных опытах с добавками воды и других веществ, за исключением опытов с добавками смолы, при температурах 10 - 40 С высок и составляет 85 - 90 % от теоретического. [42]
Эффективность процесса прививки непосредственно зависит от кинетики реакции пероксидирования при облучении. Выход перекисей определяется как значением Gp облученного вещества, так и стабильностью образовавшейся перекиси при температуре облучения. Однако детальные исследования механизма образования перекисей пока еще очень малочисленны. [43]
Когда R является хлором, реакция легко протекает на холоду в эфирном растворе; в этом случае нет необходимости добавлять в систему вещества основного характера. Выход перекиси достигает 61 - 67 %, считая на этил - или грет-бутилгидропере-кись. Лучший выход ( 52 - 94 %) был получен для 1-этоксиизохромана. [44]
Страницы: 1 2 3 4