Ион - пиридиние
Cтраница 2
Из приведенных данных видно, что константа диссоциации иона пиридиния претерпела незначительные изменения, а уксусной кислоты уменьшилась в 105 раз. Возможно, что такое различие обусловлено не только меньшей способностью метилового спирта по сравнению с водой к образованию водородной связи, но и тем, что при диссоциации уксусной кислоты ( нейтральная частица) образуется два иона, а при ионизации пиридиний-иона число их не меняется, и метиловый спирт, имеющий меньшую диэлектрическую проницаемость, обладает худшей сольватирующей способностью, чем вода, по отношению к ацетат-аниону. [16]
При адсорбции на бренстедовских кислотных центрах в спектрах наблюдаются полосы поглощения иона пиридиния, а при адсорбции на льюисовских кислотных центрах - полосы поглощения координационно-связанного пиридина. [17]
На рис. 60 представлены спектры пиридина, комплекса пири-дин-тригидрид бора и иона пиридиния. [18]
Рассуждения относительно введения второго заместителя справедливы и для первого замещения пиридина, иона пиридиния и М - окиси пиридина. [19]
Интенсивность полосы поглощения ОН-групп при 3650 см 1 уменьшается, а интенсивность полосы поглощения иона пиридиния при 1540 см 1 увеличивается пропорционально количеству адсорбированного вещества. [20]
Данные табл. 5.3 показывают, что донорные заместители увеличивают основность пиридинового азота ( уменьшают кислотность ионов пиридиния), тогда как акцепторные уменьшают основность. Аналогичный эффект должен наблюдаться и для 3 - МЙ2 - группы. Идеальная корреляция основности 3-аминопиридина с константой а, по-видимому, чисто случайна. [21]
В воде образуются ионы гидроксония, в уксусной кислоте - ацилониевые ионы, в пиридине - ионы пиридиния. Но протонной активности может быть оценена способность растворенной кислоты передавать свой протон молекуле растворителя. Однако протонная активность сольватированного протона может отличаться от протонной активности растворенной кислоты. Это тесно связано с основностью растворителя. Ганч [351] считал, что константа диссоциации, измеренная в воде, не может быть точной мерой силы кислот; сила кислоты и электролитическая диссоциация не всегда изменяются параллельно. Спектры поглощения в ультрафиолетовой области для ряда кислот в диэтиловом эфире ( в этом случае кислоты проявляют себя как слабые кислоты) отличаются от спектров в растворителях, в которых они ведут себя как сильные кислоты. [22]
Таким образом, проведенное исследование экспериментально подтвердило, что из двух форм поверхностных соединений образующихся на катализаторе ион пиридиния подвергается более легкому гидроге-нолизу. В то же время на этом катализаторе, в отличие от катализатора, прог. По-видимому, это можно объяснить тем, что в условиях реакции освободившийся в результате гидрстснолиза протонодснорнкй центр образует ионную связь с пиридином ранее связанным координационной связью. В результате наблюдается уменьшение интенсивности полос координациошюсвязанного пиридина; по-видимому, его гидрирование происходит через стадию образования иона пиридиния. [23]
В случае цеолитов Y, обмененных на катионы щелочноземельных металлов и редкоземельных элементов, интенсивность полосы поглощения ионов пиридиния повышается пропорционально степени ионного обмена. [24]
В работах [22, 24] отмечено, что предварительная адсорбция воды окисью алюминия не приводит к появлению полос поглощения ионов пиридиния. Принимается [22], что полоса поглощения 1457 см-1, проявляющаяся как плечо у полосы 1453 см-1 ( см. рис. 115), принадлежит молекулам пиридина, связанным с более слабыми апротолными центрами поверхности. Откачка образца при 565 С приводит к удалению молекул пиридина, связанных с этими слабыми апротонными центрами, и оставляет в спектре только полосу поглощения 1459 см-1 молекул пиридина, взаимодействующих с более сильными апротонными центрами. [25]
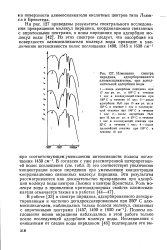 |
Изменение спектра пиридина, адсорбированного алюмисиликагелем, при дополнительной адсорбции воды. [26] |
В согласии с уже рассмотренной интерпретацией полос поглощения ( см. табл. 3) это соответствует увеличению концентрации ионов пиридиния при уменьшении концентрации координационно связанных молекул пиридина. Эти результаты рассматриваются как доказательство превращения при адсорбции молекул воды центров Льюиса в центры Бренстеда. [27]
Так как сопряженные кислоты индикаторов, приведенных в табл. 9.5, на много порядков менее кислы, чем ионы пиридиния, они должны образовывать с анионом более прочную водородную связь. [28]
В спектрах пиридина, адсорбированного на цеолитах со щелочными катионами, не обнаружено полос поглощения, характерных для ионов пиридиния. Это служит еще одним доказательством отсутствия на этих цеолитах бренстедовской кислотности. Среди цеолитов со щелочными катионами наиболее подробно исследованы натриевые формы цеолитов X и Y. Особое внимание при этом уделено выяснению вопроса о наличии кислотных центров на поверхности этих цеолитов. [29]
В спектре адсорбированного алюмосиликатным катализатором пиридина наблюдается, кроме того, полоса поглощения 1540 см - характерная для иона пиридиния и указывающая на существование на поверхности кислотного центра типа Бренстеда. [30]
Страницы: 1 2 3 4