Ион - пиридиние
Cтраница 3
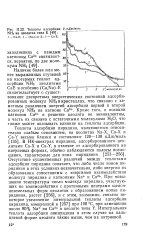 |
Теплоты адсорбции 1 кДк1моль NH3 на цеолитах типа Е. [31] |
При повышении температуры число молекул пиридина, участвующих во взаимодействии с протонными центрами щелочноземельных форм цеолитов с образованием ионов пиридиния, растет 256 ], и с этим, возможно, связано некоторое увеличение интегральной теплоты адсорбции пиридина, измеренной в [257] при 100 С, при замещении около 80 % Na на Са2 в цеолите типа Y. [32]
Различие а - и [ 3-форм ( PyH) 2H2Re28rs заключается в различной степени упорядоченности расположения ( ориентации) ионов пиридиния. [33]
В работах [3, 74] было обнаружено, что в присутствии пиридина, адсорбированного на дегидроксилированных фожазитах, при добавлении воды появляются ионы пиридиния. Этот результат не является доказательством обратимости реакций ( 11) и ( 13а); его можно объяснить тем, что катионы ( включая группировки АЮ), компенсирующие отрицательный заряд каркаса, вызывают диссоциацию адсорбированных молекул воды [ в соответствии с реакциями ( 2 - 6) ], образуя дополнительное число протонов. [34]
Это предположение основывалось на том, что значение частоты этого колебания у пиридина, координационно связанного с центром Льюиса, иона пиридиния и пиридина, адсорбированного молекулярно, одинаково и лишь немного отличается от частоты поглощения невозмущенной молекулы пиридина. [35]
Характерные отличия в области 1400 - 1700 см 1 наблюдаются в спектре пиридина, адсорбированного за счет водородных связей, ионов пиридиния и координационно связанного с электрофильными центрами пиридина. При этом доказательства существования брен-стедовских центров на поверхности окиси алюминия не были получены, в то время как присутствие льюисовских центров не вызывало сомнения. [36]
На основании спектрофотометрических исследований эти значения были приписаны: p / Cf - фенольному протону и р / С2 - протону иона пиридиния. [37]
В буферном растворе уксусной кислоты и ацетата натрия рН изменяется при нагревании лишь незначительно, тогда как в буферном растворе, содержащем ионы пиридиния и пиридин, при нагревании происходит уменьшение рН ( увеличение Кп) - Поэтому метиловый красный, интервал рН которого не чувствителен к температуре, дает лишь незначительное изменение окраски в ацетатном буфере, однако переходит в свою кислую форму при нагревании в пиридиновом растворе. [38]
Поскольку вполне определенно установлено, что нитрование в серной кислоте происходит за счет иона нитрония NO [18], становится ясным, что нитрование уже заряженного положительно иона пиридиния должно быть затруднено и идти не в положения 2 и 4 с низкой электронной плотностью, а в положение 3, которое подвергается относительно более слабому воздействию аммонийного кольцевого атома азота пиридиния. Подобйое рассуждение справедливо и для других случаев взаимодействия пиридина с другими положительными или электрофильными реагентами, например для сульфирования, бромирования или для реакции Фриделя - Крафтса. [39]
Согласно толкованию этого явления ( которое лучше всего согласуется с кинетическими данными и дает объяснение пространственному эффекту), предполагается, что в реакции кислоты с ионом пиридиния участвует молекула растворителя. Комбинация кислоты, иона пиридиния и пиридина ( растворителя) приводит, как показано ниже, к образованию промежуточного соединения XXIII, в котором протон и молекула растворителя присоединились по а, 3-двойиой связи. [40]
Поскольку последние в основном определяются распределением зарядов, параметры Паризера - Парра выбирались так, чтобы приближенно воспроизвести распределения зарядов на атомах в пиридине и в ионе пиридиния, найденные экспериментально методом ЯМР. Полученные таким образом параметры использовались для других сходных с пиридином молекул. [41]
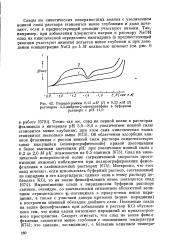 |
Подпрограммы 0 12 мМ ( 1 и 0 23 мМ ( 2. [42] |
Выравнивание спада в пиридиновом буферном растворе связано, очевидно, со значительным снижением абсолютной величины отрицательного - потенциала в присутствии ионов пири-диния, а также с участием донора протонов ( ионов пиридиния) в построении внешней обкладки двойного слоя. Появление спада на волне фенолфталеина при добавлении в раствор КС1 обусловлено тем, что ионы калия вытесняют пиридиний из приэлектрод-ного пространства. [43]
Выравнивание спада в пиридиновом буферном растворе связано, очевидно, со значительным снижением абсолютной величины отрицательного т - потенциала в присутствии ионов пири-диния, а также с участием донора протонов ( ионов пиридиния) в построении внешней обкладки двойного слоя. Появление спада на волне фенолфталеина при добавлении в раствор КС1 обусловлено тем, что ионы калия вытесняют пиридиний из приэлектрод-ного пространства. [44]
Пиридин образует устойчивые соли с сильными кислотами и часто применяется для нейтрализации кислоты, образующейся при реакции, или в качестве растворителя основного характера. Ион пиридиния может стабилизировать необычные анионы; например, известны тетрахлорборат ( BCLT) [4] и гидродихлорид ( HClf) пиридиния. Это объясняется, вероятно, гибридизацией связей атома азота: в аммиаке свободная электронная пара находится на 5р3 - орбите, а в пиридине - на зр2 - орбите ( ср. [45]
Страницы: 1 2 3 4