Ион - пиридиние
Cтраница 4
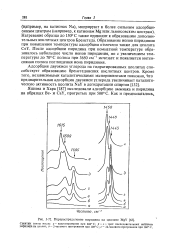 |
Перераспределение пиридина на цеолите KfgY. [46] |
Нагревание образца до 150 С также приводит к образованию дополнительных кислотных центров Бренстеда. Образование ионов пиридиния при повышении температуры адсорбции отмечено также для цеолита CeY. После адсорбции пиридина при комнатной температуре образовалось небольшое число ионов пиридиния, но с увеличением температуры до 70 С полоса при 3650 см 1 исчезает и появляется интенсивная полоса поглощения иона пиридиния. [47]
Реакционная способность по отношению к нуклеофилам усиливается при наличии подходящим образом расположенных электроноакцепторных групп, таких, как N02, COOR и S03R, а также при переводе атома азота пиридина в четвертичное состояние. Действительно, ионы пиридиния, несущие заместитель, проявляющий сильный - Af-эффект, склонны вступать в реакции раскрытия кольца при нуклеофильной атаке разными реагентами - реакции, не встречающиеся среди нитропроизводных бензола. Несмотря на это, замещенные пиридины напоминают производные бензола тем, что при их реакциях может обмениваться не только водород, но и другие группы. [48]
Реакционная способность по отношению к нуклеофилам усиливается при наличии подходящим образом расположенных электроноакцепторных групп, таких, как N02, COOR и S03R, а также при переводе атома азота пиридина в четвертичное состояние. Действительно, ионы пиридиния, несущие заместитель, проявляющий сильный - ЛГ-эффект, склонны вступать в реакции раскрытия кольца при нуклеофильной атаке разными реагентами - реакции, не встречающиеся среди нитропроизводных бензола. Несмотря на это, замещенные пиридины напоминают производные бензола тем, что при их реакциях может обмениваться не только водород, но и другие группы. [49]
На рис. 1 показаны ИК-спектры пиридина, адсорбированного на NaX и LaX. Характеристическая полоса иона пиридиния в области 1540 см 1 не обнаруживается. Это показывает, что в цеолите NaX большинство кислотных центров являются льюисов-скими кислотами. Полоса 1445 см-1 не изменяется при введении в систему воды. [50]
Каталитические константы для кислот в водном растворе хорошо коррелируют с р / С, причем заметного различия между незаряженными и катионными кислотами ( карбоновые кислоты и катионы пиридиния) не наблюдается. Для 2 6-замещенных ионов пиридиния наблюдается некоторое замедление реакции вследствие стерических факторов. Каталитические константы для оснований несколько менее точны, и, как показали Грюн и МакТигью [49], ошибка обусловлена методом измерения скоростей реакций по образованию продуктов присоединения между ацетальдегидом и анионом катализатора. Можно отметить, что более ранние измерения при 0 дилатометрическим методом [ 10J дали лучшую корреляцию между kb и р / С семи оснований различных типов, поэтому необходимы дальнейшие исследования. [51]
Согласно толкованию этого явления ( которое лучше всего согласуется с кинетическими данными и дает объяснение пространственному эффекту), предполагается, что в реакции кислоты с ионом пиридиния участвует молекула растворителя. Комбинация кислоты, иона пиридиния и пиридина ( растворителя) приводит, как показано ниже, к образованию промежуточного соединения XXIII, в котором протон и молекула растворителя присоединились по а, 3-двойиой связи. [52]
Страницы: 1 2 3 4