Вычисление - константа - скорость
Cтраница 1
Вычисление констант скорости хим. р-ций упрощается, если в неравновесной в целом системе можно выделить равновесные подсистемы. Константы скорости р-ций в таких случаях выражаются как ф-ции т-р подсистем. Тт входит Г ол, а предэкспоненциальный множитель слабо зависит от т-ры. Для молекул, состоящих из неск. [1]
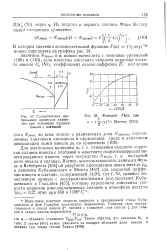 |
Схематическое изображение процессов диффузии при окислении сплавов никеля с платиной. [2] |
Вычисление констант скорости коррозии в оригинальной статье Куба-шевского и фон Гольдбек произведено неправильно. [3]
Вычисление константы скорости реакции производят по уравнению ( XVIII, За), а для выражения отношения концентраций в нем пользуются свойством оптической деятельности растворов. [4]
Вычисление константы скорости спонтанного распада при фиксированных значениях внутренней энергии и вращательного момента или только внутренней энергии молекулы, а также другие наиболее емкие математические выкладки § 16, 29 и 31 вынесены в конец книги в виде четырех Приложений. [5]
При вычислении константы скорости объем системы обычно предполагают постоянным. В случае систем с непостоянным объемом необходимо вносить соответствующие поправки. В частности, это важно для опытов с ударной трубой и для струевых систем, если реакция в заметной степени экзотермична или эндо-термична. [6]
При вычислении константы скорости простой реакции необходимо учитывать два обстоятельства: помнить, по какому реагенту измеряется скорость реакции и чему равен порядок реакции по этому реагенту. [7]
 |
Коэффициенты пересчета для k второго порядка.| Коэффициенты пересчета для k третьего порядка. [8] |
При вычислении константы скорости простой реакции необходимо учитывать два обстоятельства: помнить, по какому реагенту измеряется скорость реакции и чему равен стехиометрическии коэффициент и порядок реакции по этому реагенту. [9]
Ясно, что вычисление константы скорости по обычной формуле дает закономерно падающие значения К. [10]
Здесь излагается метод вычисления константы скорости на основе схемы, в которую наряду с колебательными переходами включена вращательная диссоциация из различных колебательных состояний молекулы. При вычислении константы скорости диссоциации принята во внимание взаимосвязь заселенностей колебательных состояний со скоростью переходов из них. [11]
Решение обратной задачи - вычисление константы скорости из экспериментальных данных может быть выполнено графически, так как тангенс угла наклона прямой, изображенной на рис. 87, равен константе скорости. [12]
Решение обратной задачи - вычисление константы скорости из экспериментальных данных может быть выполнено графически, так как тангенс угла наклона прямой, изображенной на рис. 87, равен константе скорости. [13]
Теоретическая химическая кинетика занимается вычислением констант скорости химических реакций исходя из строения и свойств исходных частиц и опираясь на методы квантовой химии и статистической физики. [14]
Таким образом, при вычислении констант скоростей бимолекулярных реакций правильнее использовать значения слок, поскольку подстановка в кинетические уравнения величины с приводит к завышенным значениям констант скоростей. Не исключено также, что повышение локальных концентраций в твердой фазе по сравнению с жидкостью вызывает иногда кажущееся ускорение твердофазных реакций при низких температурах. [15]
Страницы: 1 2 3 4