Ион - торий
Cтраница 1
Ионы тория с арсеназо III образуют окрашенное и прочное соединение. Это позволяет определять торий в сильнокислых растворах без отделения сульфатов, фосфатов, фторидов, оксалатов и других ионов. [1]
Ион тория, благодаря малому радиусу и большому заряду, прочно удерживается катионообменными смолами, что обусловливает возможность отделения тория от многих других ионов путем сорбции на ионообменной колонке с последующим вымыванием более слабо связанных ионов соответствующим десор-бентом. [2]
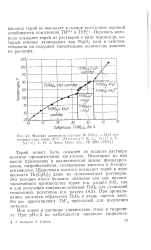 |
Фазовая диаграмма системы Th ( NOsi - H2O при. [3] |
Ион тория в растворе удивительно стоек к гидролизу. При рН3 не наблюдается никакого гидролиза. [4]
Ион тория в заметной степени комплексуется почти всеми анионами. Равновесные константы комплексооб-разования тория с простыми неорганическими анионами приведены в табл. 4.2. Торий образует анионные комплексы в растворах карбонатов и оксалатов щелочных металлов, а также растворимые в органических растворителях комплексы со многими циклообразующими агентами, в том числе с дикетонами и производными 8-гидроксихинолина. В этих комплексах с каждым ионом тория связаны четыре хелатные группы. [5]
Ионы тория на монофункциональной иминодиуксусной смоле в противоположность монофункциональной саркозиновой смоле поглощаются лишь в незначительных количествах, причем еще не ясно, объясняется ли это процессом комплексообразования или адсорбцией продуктов гидролиза. Th ( NO3) 4 ( рН 2 7) и комнатной температуре адсорбируется 0 04 моля Th4 на 1 моль монофункциональной иминодиуксусной смолы. [6]
Затем ионы тория элюи-руют растворами, в которых последний образует анионные комплексы, например, щавелевой или серной кислотой. [7]
Предварительно отделяют ионы тория от ионов хлора, чтобы первые не мешали аргентометрическому определению хлора. Для этого две небольшие стеклянные колонки бюреточного типа заполняют 10 г катионита КУ-2 в Na-форме. [8]
Реактив на ионы тория, урана ( IV), цинка, циркония, тантала, ниобия, редкоземельных элементов, висмута, нептуния, хрома ( II) - в кислой среде. [9]
Определению мешают ионы тория, висмута, циркония, алюминия, марганца, меди, хрома и никеля, соединения молибдена, ванадия, иода. [10]
Изучение поведения иона тория на ртутном капельном электроде показало, что его восстановление происходит лишь при значениях рН около 3 6, когда начинается гидролиз тория. [11]
Анализ смеси ионов тория и кобальта, Ионы кобальта открывают на бумаге. На бумагу наносят одну-две капли исследуемого раствора, затем одну-две капли воды и раствора а-нитрозо-8 - нафтола, В центре появляется пурпурно-красное пятно, свидетельствующее о присутствии ионов кобальта. Внешние края пятна проявляют ализарином. В присутствии ионов тория образуется фиолетовая зона, не исчезающая в уксусной кислоте. [12]
Установлено, что ионы тория взаимодействуют с 5 7-дибром - 8-оксихинолином ( ДБО) и родамином С ( RhC) с образованием нефлуоресцирующего ионного ассоциата, экстрагируемого бензолом. Сделаны предположения о механизме его образования и флуоресцентных свойствах. Предложен экстракционно-флуориметрический метод определения тория по тушению флуоресценции. [13]
Дибензоилметан осаждает также ионы тория ( IV) при рН 4 - 5 в виде соединения12 Th ( Ci5HnO2) 4 и применяется для отделения тория от церия ( III), лантана и лантанидов. [14]
Бензоилфенилгидроксиламин количественно осаждает ионы тория при рН 2 в виде кристаллического осадка белого цвета. Осадок устойчив при нагревании до 220 С. [15]
Страницы: 1 2 3 4