Ониевый ион
Cтраница 2
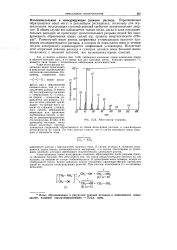 |
Масс-спектр н-декана. [16] |
С-С-X может распадаться как с образованием ониевого иона, так и с отщеплением алкила. В первом случае разрывается соседняя с гетероатомом С-С - связь, во втором - гетероатом отщепляется как радикал. Какая из этих реакций преобладает, это прежде всего зависит от строения углеродного скелета ( образование вторичных или третичных карбониевых ионов. [17]
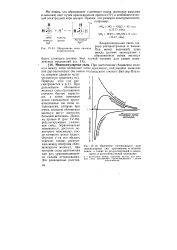 |
Изменение интенсивности межмолекулярных сил притяжения и отталкивания, а также их результирующей в зависимости от расстояния между частицами. [18] |
Мы видим, что образование - ониевых ионов ( катионов аммония и оксония) идет путем присоединения протона ( Н) к необобществленной электронной паре донора. [19]
Принимая протон, молекула воды превращается в ониевый ион, называемый по-разному - гидроний-ион, оксоний-ион, гидроксоний-ион. По химическому составу его правильнее всего называть гидроксонием, так как это ониевый ион, ядром которого является атом кислорода ( окс-атом), а лигандами - атомы водорода. Однако, так как этот ион - лионий-ион, к тому же образуемый таким главным растворителем, как вода, то целесообразней и проще называть его гидроний-ионом. [20]
Термин карбоний предполагает, что ионы карбония аналогичны другим ониевым ионам ( аммоний, фосфоний, оксоний, сульфоний, иодоний и другие), и именно эту аналогию имел в виду Байер [36], предложивший этот термин. Однако сходство между этими ионами не распространяется далее наличия положительного заряда в каждом из них. Аммониевые ионы образуются при взаимодействии амина, являющегося донором пары электронов, с акцептором этой пары - протоном. Точно так же фосфор ( III), кислород, сера и иод обладают свободной парой электронов, которые участвуют в образовании ониевых комплексов. Это возражение против термина карбоний было сразу же высказано Гомбергом [581], предложившим называть соли этих ионов солями карбила, но этот термин не был принят. [21]
Таким образом, в процессе присоединения протона возникает новая кислота - ониевый ион, соответствующий основанию. [22]
Следовательно, кислотность при этом возрастает и становится выравненной и появляется ониевый ион, который и титруют. [23]
Не вызывает сомнения тот факт, что в мономолекулярных реакциях элиминирования ониевые ионы и галогениды в противоположность реакциям бимолекулярного элиминирования ведут себя одинаковым образом. При бимолекулярных реакциях конкурирующие формы атаки на ониевые ионы и на галогениды приводят к различным по существу продуктам, а при мономолекулярных реакциях как из ониевого иона, так и из галогенида первоначально образуется карбониевый ион, который подвергается конкурирующим между собой атакам. Однако количественно ориентация по Зайцеву более резко выражена при мономолекулярных реакциях элиминирования от ониевых ионов и галогенидов, чем при бимолекулярных реакциях отщепления из галогенидов. [24]
Ониевые ионы играют важную роль в неводном титровании: молекулы амфотерных растворителей образуют ониевые ионы при протонировании. Примером может служить ацилониевый ион CHgCOOHj. По Бренстеду все эти соединения являются катионными кислотами. Кислотность катионных кислот находится в обратной зависимости от основности сопряженных оснований. [25]
Электрофильное замещение при гетероатомах начинается электрофиль-ной атакой свободной электронной пары п с образованием промежуточного ониевого иона, после чего следует катионоидный отрыв остатка, ранее связанного с гетероатомом. [26]
Согласно наиболее распространенной точке зрения, по-видимому, первоначальное взаимодействие молекул галогена и алкена дает плоский циклический ониевый ион, например хлороний - или бромоний-ион, структура которого допускает нуклеофильную атаку по одному из атомов углерода только со стороны, противоположной вхождению атома галогена. [27]
По-видимому, это одна из промежуточных точек того континуума переходных состояний, крайние позиции в котором занимают симметричный ониевый ион и тримолекулярное переходное состояние, когда нуклеофил - ихэлектрофил, не будучи связаны между собой, раздельно, но существенно одновременно атакуют двойную связь ( см. стр. [28]
Последние авторы предположили, что стабилизация посредством сверхсопряжения имеет место во всех случаях, однако при распаде ониевых ионов определяющими являются пространственные факторы. [29]
Увеличение электронной плотности на гетероатоме за счет индукционного влияния алкильных групп также сказывается на повышении интенсивности пиков ониевых ионов. [30]
Страницы: 1 2 3 4