Ацетатный ион
Cтраница 2
Так как соль полностью диссоциирована, то концентрация ацетатных ионов равна концентрации солисснсоо - ссоли. [16]
Нитрат лантана дает с иодом, аммиаком и ацетатными ионами красивый темносвдий осадок, который, вероятно, обусловливается адсорбцией иода основным а - етатом лантана. Если присутствуют фосфаты Н - ти сульфаты, последние лучше всего удалить, осадив их нитратом бария. [17]
Нитрат лантана дает с иодом, аммиаком и ацетатными ионами красивый темносвдий осадок, который, вероятно, обусловливается адсорбцией иода основным ацетатом лантана. [18]
Перрен [8], изучая систему ферро - ферри - ацетатный ион, не обнаружили присутствия в исследуемых растворах всех форм комплексных соединений железа, существование которых доказано нами. Безусловно, это сказывается на численных значениях констант образования. Во-вторых, различные условия ( концентрация железа, ионная сила и температура), при которых производились определения констант образования, также являются причиной наблюдаемого различия в значениях некоторых констант. Вге это не позволяет провести строгого сравнения приведенных в табл. 2 данных. [19]
Вторая стадия - диссоциация образовавшегося диазоаце-тата на арилдиазоний и ацетатный ион - протекает быстро. [20]
При введении в раствор уксуснокислого натрия CH COONa концентрация ацетатных ионов СН3СОО - в растворе сильно увеличивается, вследствие ионизации этой соли, и равновесие диссоциации уксусной кислоты сместится в левую сторону. [21]
Целью настоящей работы является подробное исследование системы ферри - ферро - ацетатный ион и доказательство на примере этой системы применимости метода окислительного потенциала [14, 15] для исследования систем, в которых возможно образование, кроме одноядерных, также смешанных многоядерных комплексов. [22]
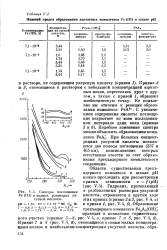 |
Спектры поглощения Fe ( III в водных растворах уксусной кислоты. [23] |
Кривые 2 ж 3, относящиеся к растворам с небольшой концентрацией ацетатных ионов, пересекаясь друг с другом, а также с кривой 1, образуют изобестическую точку. [24]
Различие между этим и предыдущим уравнением заключается только в том, что ацетатный ион имеет заряд - 1, тогда как молекула аммиака представляет собой нейтральную частицу. Однако это различие не должно скрыть от нас сходства в кислотно-основном поведении водных растворов в том и другом случае. [25]
Способ действия буферного раствора, например раствора уксусной кислоты, в присутствии ацетатного иона следующий: если водородный ион в виде сильной кислоты прибавляется к буферному раствору, ацетатный ион соединяется с ним, образуя уксусную кислоту. Поскольку уксусная кислота диссоциирует слабо, концентрация водородного иона не изменится в заметной степени. [26]
В тексте подлинника имеются некоторые особенности, которые мы сохранили, например, ацетатный ион сокращенно обозначают Ас -, формулы в тексте, взятые в скобки, обозначают концентрацию и пр. Небольшие дополнения редактора в тексте взяты в звездочки. [27]
Изучение зависимости окислительного потенциала системы ферри - ферро от равновесной активности адденда ( ацетатных ионов), приведенное в настоящей работе, подтвердило предполагаемый состав комплексов железа. [28]
Это объясняется тем, что при прибавлении кислоты ее ионы Н связываются с ацетатными ионами соли в недиссоциированные молекулы уксусной кислоты, а если прибавляется щелочь, то она связывается уксусной кислотой в соответствующий ацетат. [29]
Это объясняется тем, что при прибавлении кислоты ее ионы Н связываются с ацетатными ионами соли в недиссоции-ро Ванные молекулы уксусной кислоты, а если прибавляется щелочь, то она связывается уксусной кислотой в соответствующий ацетат. [30]
Страницы: 1 2 3 4