Ацетатный ион
Cтраница 3
Так, например, для уксусной кислоты АО равно сумме электропроводностей иона водорода и ацетатного иона; электропроводность иона водорода определяется из данных для сильных кислот, а электропроводность ацетатного иона - на основании исследования растворов ацетатов. [31]
Так как при диссоциации водородный и ацетатный ионы образуются в равных количествах, то концентрация ацетатного иона также будет составлять 6 00132 моля на литр. [32]
С-О будут различными, вызывающими тем самым большее разделение двух частот валентных колебаний СО, чем наблюдается в свободном ацетатном ионе. Однако, если ацетатный ион служит бидентатным мостиком, например в [ Си2 ( СН3СОО) 4 ( Н20) 2 ], значительного разделения частот ожидать не приходится. [33]
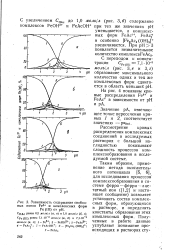 |
Зависимость содержания свободных ионов Fe3 и комплексных форм. [34] |
Таким образом, применение метода окислительного потенциала [5, 6], для исследования процессов комплексообразования в системе ферро - ферри - ацетатный ион ( [1,2] и настоящее сообщение) позволяет установить состав комплексных форм, образующихся в растворе, и определить константы образования этих комплексных форм. [35]
Следует подчеркнуть, что в эти вытяжки переходит часть органического вещества, мешающего определению марганца, кроме того, присутствие ацетатного иона затрудняет анализы, в связи с чем необходимо полностью разрушить органическое вещество и ацетаты. Разрушение проводят как многократной обработкой азотной кислотой и перекисью водорода при нагревании, так и прокаливанием выпаренного досуха остатка вытяжки после предварительного окисления азотной кислотой и перекисью водорода. [36]
Ас - ] приблизительно равна 1М 1 так как при диссоциации сильного электролита, уксуснокислого натрия, получается один моль иона натрия и один моль ацетатного иона. [37]
В действительности немного более 1М, так как ацетатный ион также получается при диссоциации уксусной кислоты, но этой величиной можно пренебречь по сравнению с концентрацией ацетатного иона, получающегося из уксуснокислого натрия. [38]
Способ действия буферного раствора, например раствора уксусной кислоты, в присутствии ацетатного иона следующий: если водородный ион в виде сильной кислоты прибавляется к буферному раствору, ацетатный ион соединяется с ним, образуя уксусную кислоту. Поскольку уксусная кислота диссоциирует слабо, концентрация водородного иона не изменится в заметной степени. [39]
Прибавление небольших количеств сильной кислоты или щелочи тоже сравнительно слабо отражается на рН Это оГъя - нягтся тем, что при прибав-лении кислоты ее ионы Н связываются с ацетатными ионами соли в недис-социиров энные молекулы уксусной кислоты, а если прибавляется щелочь, то она связывается уксусной кислотой в соответствующий ацетат. [40]
Нетрудно понять, что раствор, содержащий равное число эквивалентов NaOH и НС2Н3О2, не будет иметь рН 7, а окажется слегка основным из-за происходящего в нем гидролиза ацетатных ионов. [41]
Так, например, для уксусной кислоты АО равно сумме электропроводностей иона водорода и ацетатного иона; электропроводность иона водорода определяется из данных для сильных кислот, а электропроводность ацетатного иона - на основании исследования растворов ацетатов. [42]
Из табл. 18 действительно видно, что Ан / А а1 во всех случаях где реакция катализируется не только ионами водорода или гидроксила сильных кислот или оснований, но и недиссоциированными молекулами или ацетатным ионом. [43]
В случае прибавления к буферным растворам небольших количеств сильной кислоты или основания рН этих растворов меняется сравнительно слабо, так как при прибавлении кислоты к ацетатному буферному раствору ее ионы Н связываются с ацетатными ионами соли в малодиссоциированную уксусную кислоту, а при добавлении щелочи она связывается уксусной кислотой в соответствующий ацетат. Количественной характеристикой буферных свойств растворов является буферная емкость, которая может быть измерена количеством кислоты или щелочи ( в г-экв), при добавлении которых к раствору рН раствора меняется на единицу. [44]
В случае прибавления к буферным растворам небольших количеств сильной кислоты или основания рН этих растворов меняется сравнительно слабо, так как при прибавлении кислоты к ацетатному буферному раствору ее ионы Н связываются с ацетатными ионами соли в малодиссоциированную уксусную кислоту, а при добавлении щелочи она связывается уксусной кислотой в соответствующий ацетат. [45]
Страницы: 1 2 3 4