Молекулярный ион - водород
Cтраница 1
 |
Энергетика образования связи в молекуле Н2. а-кривая потенциальной энергии молекулы с электронами на связывающей орбитали, имеющая минимум при экспериментально наблюдаемом. [1] |
Молекулярный ион водорода Н2 имеет два ядра ( протона), но всего один электрон. По соображениям Паули, этот электрон должен находиться на молекулярной орбитали с самой низкой энергией, а согласно рис. 12 - 5 6, это должна быть связывающая а-орбиталь. Молекулярный ион HJ должен быть слабоустойчивым. [2]
Молекулярный ион водорода играет такую же роль в теории молекул, как атом водорода - в теории атома, так как для иона HJ в приближении Борна - Оппенгеймера электронное волновое уравнение может быть решено точно. ЛКАО, которые послужат нам основой для рассмотрения двухатомных гомоядерных молекул. [3]
Молекулярный ион водорода состоит из двух протонов и одного электрона. Состояние 1 соответствует локализации электрона вблизи одного протона, а состояние 2 - локализации вблизи другого протона. [4]
 |
Уменьшение электронной плотности с увеличением расстояния от ядра в атоме водорода в основном состоянии. [5] |
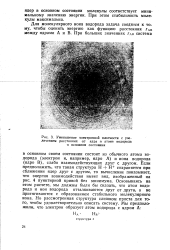
Для молекулярного иона водорода задача сводится к тому, чтобы оценить энергию как функцию расстояния ГАВ между ядрами А и В. [6]
Так называемый молекулярный ион водорода HJ состоит из двух протонов и одного электрона. В данном случае образуется частица, в которой связь обусловлена не электронной парой, а единственным электроном. [7]
 |
Взаимодействие атомных орбиталей атомов водорода. а - неперекрывающиеся орбитали. б - перекрывающиеся орбитали. [8] |
В случае молекулярного иона водорода возможно точное решение уравнения Шредингера: известны набор волновых функций для электрона и разрешенные значения энергии этой системы. Однако здесь будет рассмотрено приближенное, но зато более наглядное решение этого вопроса. [9]
Рассматривая проблему молекулярного иона водорода в приближении МО ЛКАО, мы приходим к ясному представлению о построении молекулярных орбиталей из атомных. Оказывается, что связывающая орбиталь возникает при сложении атомных орбиталей, а разрыхляющая - при их вычитании. В основном состоянии молекулярного иона водорода заполненной оказывается связывающая орбиталь. [10]
Расчет фотодиссоциации молекулярного иона водорода приведен в работе [241 ], где отмечается, что для сравнения с экспериментом нужны дополнительные экспериментальные данные. [11]
В случае молекулярного иона водорода возможно точное решение уравнения Шредингера: известны набор волновых функций для электрона и разрешенные значения энергии этой системы. Однако здесь будет рассмотрено приближенное, но зато более наглядное решение этого вопроса. [12]
Только для молекулярного иона водорода Нг известно точное решение волновомеханического уравнения Шредингера. [13]
Поэтому в молекулярном ионе водорода электрон находится на связывающей орбитали. В более сложных системах заполнение разрыхляющих орбиталей очень важно для определения характера связи. [14]
Такой системой является молекулярный ион водорода Н, состоящий из двух ядер водорода и одного электрона. [15]
Страницы: 1 2 3 4