Молекулярный ион - водород
Cтраница 3
Простейшей из всех молекул является молекулярный ион водорода Но, состоящий из двух протонов и одного электрона. Хотя этот ион обнаружен только спектроскопически, он обладает значительной стабильностью, поскольку энергия, потребная для диссоциации на протон и нейтральный атом водорода, составляет около 61 ккал / моль. Но для наших целей более полезен чисто качественный подход, использующий концепцию резонанса. [31]
 |
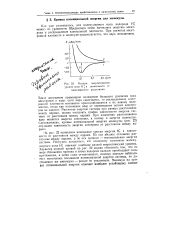
Зависимость энергии волновых функций я з и 1 - от межъядерного расстояния в молекулярном ионе водорода. [32] |
Следует отметить, что для молекулярного иона водорода оба метода - и простой метод молекулярных, орбиталей, и метод валентных связей - приводят к одинаковым значениям энергии и длины связи. А и идентична одной из исходных атомных орбиталей ( ФА) метода ЛКАО; аналогично ори идентична фв. В обоих методах используются линейные комбинации, но в методе валентных связей комбинируются гипотетические структуры, а в методе молекулярных орбиталей используются обычные одноэлектронные функции - атомные орбитали. Для более сложных молекул функции, из которых образуются линейные комбинации, уже не будут одни и те же в обоих методах, и тогда разница между двумя методами станет яснее. [33]
Простой пример имеется в теории молекулярного иона водорода, для которого волновые функции строятся комбинированием атомных 15 орбит обоих атомов. Первая не изменяется ни при одной из операций симметрии, в то время как вторая не изменяется при одних операциях, таких, как вращение вокруг оси, и меняет знак при других, таких, как инверсия и отражение в плоскости, перпендикулярной оси. Если электрон находится на первой орбите, то состояние полностью симметрично, если - - на второй, то оно принадлежит неполностью симметричному представлению. [34]
 |
Низшие энергетические. [35] |
Как уже указывалось, для молекулярного иона водорода Н2 можно по уравнению Шредингера точно вычислить энергию электрона и распределение электронной плотности. При расчетах электронной плотности в молекуле предполагается, что ядра неподвижны. [36]
 |
Низшие энергетические. [37] |
Как уже указывалось, для молекулярного иона водорода Нз можно по уравнению Шредингера точно вычислить энергию электрона и распределение электронной плотности. При расчетах электронной плотности в молекуле предполагается, что ядра неподвижны. [38]
 |
Схема образования связывающей и разрыхляющей молекулярных о-орбиталей. [39] |
Нетрудно подсчитать, что в молекулярном ионе водорода и ди-гелий-ионе порядок связи равен 0 5, в молекуле водорода 1, а в системе из двух невозбужденных атомов гелия - нулю. [40]
 |
Взаимодействия в Н. [41] |
Интересно также рассмотреть взаимодействия в молекулярном ионе водорода. Конечно, точно определить положение электрона в молекуле невозможно, так же как и в атоме. Квантовая механика дает только распределение вероятности. [42]
Нетрудно подсчитать, что в молекулярном ионе водорода и ди-гглий-ионе порядок связи равен 0 5, в молекуле водорода 1, а в системе из двух атомов гелия - нулю. [43]
 |
Схема образования связывающей о7 - и разрыхляющей а - орбитаж й. [44] |
Нетрудно подсчитать, что в молекулярном ионе водорода Н и диагелий-ионе Не2 порядок связи равен 0 5, в молекуле водорода - 1, а в системе из двух невозбужденных атомов гелия - нулю. [45]
Страницы: 1 2 3 4