Молекулярный ион - водород
Cтраница 4
 |
Схема образования связывающей и разрыхляющей молекулярных о-орбиталей. [46] |
Нетрудно подсчитать, что в молекулярном ионе водорода и ди-гелий-ионе порядок связи равен 0 5, в молекуле водорода 1, а в системе из двух невозбужденных атомов гелия - нулю. [47]
Однако из расчетов, произведенных для молекулярного иона водорода и молекулы водорода, мы можем почти с уверенностью сделать вывод, что сходство между истинной функцией ф ( 1 2) и какой-либо простой формой функции Ф является в лучшем случае лишь ограниченным. [48]
Эта кривая согласуется с наблюдаемыми свойствами молекулярного иона водорода. [49]
Рассмотрим простейшую из возможных молекулярных систем - молекулярный ион водорода HJ - ( Эта частица получается при облучении молекул водорода Н2 электронами. В нем один электрон движется в поле двух ядер - протонов. [50]
С точки зрения метода МО разница между молекулярным ионом водорода и молекулой Н2 заключается в заселенности связывающей МО [ а ], на которой соответственно один и два электрона. В системах с недостатком валентных электронов, в том числе в металлах, согласно методу МО химическая связь ковалентна. Это подтверждается тем, что в решетке типичных металлов все атомы кристаллографически эквивалентны между собой и эффективные заряды атомов равны нулю. [51]
В простейшем виде ковалентная связь реализуется в молекулярном ионе водорода HJ, в котором оба протона имеют всего один общий электрон. Электростатическое отталкивание протонов стремится развалить молекулу. Но, с другой стороны, энергия связи электрона в поле двух протонов, конечно, больше, чем при наличии только одного протона. При определенном расстоянии между протонами ( 0 1 нм) второй фактор оказывается более существенным, что обеспечивает устойчивость такой системы. Еще прочнее оказывается ковалентная связь в нейтральной молекуле водорода ( 4 48 эВ), где она образуется двумя электронами. [52]
В целях квантово-механического расчета можно принять, что молекулярный ион водорода возникает из протона и атома водорода. Если эти две частицы приближаются друг к другу без изменения структуры, то вычисленная энергия взаимодействия, отложенная на графике по расстоянию между ними ( гаЬ), дает показанную на рис. 4 пунктирную кривую, из которой видно, что эти две частицы будут отталкиваться друг от друга. [53]
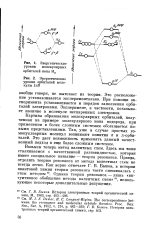 |
Энергетические уровни молекулярных орбиталей иона Н2.| Энергетические уровни орбиталей молекулы LiH. [54] |
Картина образования молекулярных орбиталей, полученная на примере молекулярного иона водорода, при применении к более сложным системам обогащается новыми представлениями. Так, уже в случае простых го-монуклеарных молекул возникают понятия а и я-орби-талей. Это дает возможность применять данный качественный подход к еще более сложным системам. [55]
Полезный обзор более ранних работ о молекуле и молекулярном ионе водорода был опубликован Паулингом [9]; рекомендуется за ссылками на литературу обратиться к этой статье. [56]
Молекула водорода имеет на один электрон больше, чем молекулярный ион водорода. Таким образом, молекула водорода имеет два электрона на самой нижней связывающей молекулярной орбитали. Энергии диссоциации молекулы и иона равны 458 5 и 269 3 кДж / моль соответственно. [57]
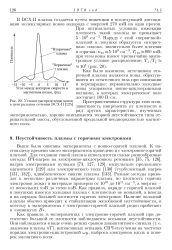 |
Угловое распределение ионов в центральном сечении DCX-II. [58] |
В DCX-II плазма создается путем инжекции и последующей диссоциации молекулярных ионов водорода с энергией 270 кэВ на один протон. [59]
В теории молекул всегда, даже в простейшем случае молекулярного иона водорода), приходится использовать приближенные методы. [60]
Страницы: 1 2 3 4