Молекулярный ион - водород
Cтраница 2
Кулоновская энергия связи молекулярного иона водорода, вычисленная по уравнению (18.18), не отличается значительно от нуля; более того, в действительности, если учитывать полученную величину, то при наличии вышеуказанного допущения полученные результаты свидетельствуют о наличии отталкивания при всех значениях междуядерных расстояний. Из этого следует, что общий эффект связи, вызываемый единственным электроном иона Н, обусловливается тем, что линейная комбинация из ид и UB будет более точно передавать собственную функцию системы, чем мд и UB, взятые в отдельности. [16]
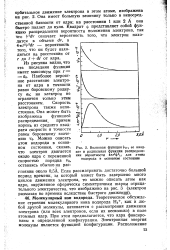 |
Волновая функция 4j s, ее квад-пат и радиальная функция распределе. [17] |
Теоретическое обсуждение строения молекулярного иона водорода Н2, как и любой другой молекулы, начинается с рассмотрения движения электрона ( или всех электронов, если их несколько) в поле атомных ядер. При этом предполагается, что ядра фиксированы в определенной конфигурации. Электронная энергия молекулы является функцией конфигурации. [18]
Для простейшего случая молекулярного иона водорода может быть найдено точное решение на основе 1ф18 - функций двух ядер водорода, находящихся бесконечно далеко друг от друга и стремящихся завладеть общим электроном. Электрон может принадлежать либо ядру 1, либо ядру 2, что дает две одинаковые волновые функции tyi и i) 2, описывающие ls - состояние водородного атома. [19]
Следующий энергетический уровень молекулярного иона водорода минимума не имеет, а потому молекула в этом состоянии образоваться не может. Энергетический уровень такого положения электрона назовем разрыхляющим и обозначим этот уровень стразр. [20]
Следующий энергетический уровень молекулярного иона водорода минимума не имеет, а потому молекула в этом состоянии образоваться не может. [21]
Как и в молекулярном ионе водорода, и по той же самой причине резонанс стабилизует систему больше всего, если ядра сближены, а не тогда, когда они удалены, и этот случай можно изобразить при помощи кривых, показывающих зависимость полной энергии от межядерного расстояния. Качественно они будут такими же, как кривые рис. 2.1, на котором кривая / изображает энергию одной нерезонирующей струк-тур. I, или II), кривая 2 показывает образование стабильного молекулярного иона, а кривая 3 соответствует сильному отталкиванию между ядрами. [22]
Существует химическая частица - молекулярный ион водорода Hjf, - в которой химическая связь образована всего одним электроном. [23]
Если представить себе образование молекулярного иона водорода из протона и атома водорода, постепенно приближающихся друг к другу, то оказывается, что единственный электрон-должен осуществлять связь между обоими протонами как атомными ядрами водорода. При решении уравнения Щредингера для системы из двух протонов и одного электрона получаются два решения, и каждое отвечает определенной величине энергии. Электрон как осуществляющий связь принадлежит всей частице как таковой и его называют находящимся на молекулярной орбитали, подобно тому как электрон в атоме находится на атомной орбитали. [24]
Сведения об электронном строении молекулярного иона водорода Н2 проливают свет на природу химической связи, подобно тому, как теоретическое исследование атома водорода помогает понять строение многоэлектронных атомов. Атомные орбитали атома водорода с учетом отталкивания электронов и принципа Паули объясняют изумительную систему, известную под названием Периодическая система, - периодическую повторяемость свойств элементов и их изменения внутри периодов. Подобным же образом при учете тех же факторов, отталкивания электронов и принципа Паули, молекулярные орбитали молекулярного иона водорода позволяют дать единое стройное объяснение многогранного явления химической связи. [25]
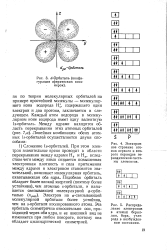 |
Электронное строение атомов первого и второго периодов периодической системы элементов.| Распределение электронов в атомах бериллия, бора, углерода в возбужденном состоянии. [26] |
Каждый атом водорода в молекулярном ионе водорода имеет одну валентную ls - орбиталь. [27]
Наиболее простой молекулярной системой является молекулярный ион водорода Н2, который обнаруживается в разрядной трубке при бомбардировке молекул водорода электронами. Энергия диссоциации такой молекулы и расстояние между ядрами водорода известны. [28]
Еще одна такая система - молекулярный ион водорода Н J, который мы обсудим ниже в связи с проблемой химической связи. [29]
Примером такой системы может служить молекулярный ион водорода Н5 при умеренных межъядерных расстояниях, когда электрон может находиться на ls - орбите у каждого из ядер. Другим примером служит молекула бензола с ее двумя структурами Кекуле. [30]
Страницы: 1 2 3 4