Комплексный ион - металл
Cтраница 1
Комплексные ионы металла не должны восстанавливаться или окисляться на поверхности электрода, обратимого по отношению к анионам. Это условие часто не выполняется. Так, например, хлоридные комплексы платиновых металлов ( PtCll, PtCl -, PdCl - и др.) самопроизвольно восстанавливаются на хлорсеребряном или каломельном электродах, и последние, как правило, нельзя использовать в качестве индикаторных электродов. [1]
Комплексный ион металла ( разд. [2]
Комплексный ион металла - система, состоящая из иона металла и определенной группы ионов или нейтральных молекул, связанных с ионом металла льюисовым кислотно-основным взаимодействием. [3]
Разряд комплексных ионов металла отличается от разряда простых аква-ионов и всегда протекает при потенциалах, более отрицательных, что связано с дополнительной затратой энергии ( со сдвигом катодного потенциала), идущей на разрушение разряжающегося комплекса. Отсюда следует, что величина подобного смещения потенциала определяется прочностью комплексного иона и концентрацией комплексообразователя. [4]
Потенциалы полуволн комплексных ионов металлов - обычно отличаются от потенциалов полуволн простых ионов. Потенциалы полуволн определены экспериментально почти для всех элементов и их можно найти в специальных таблицах. Таблица потенциалов полуволн приведена на стр. [5]
Потенциалы полуволн комплексных ионов металлов отличаются от названных величин для простых ионов; это явление подробно рассмотрено далее. [6]
Потенциалы полуволн комплексных ионов металла отличаются от потенциалов полуволн простых ( гид-ратированных) ионов металла. Потенциалы полуволн определены экспериментально почти для всех элементов, и их можно найти в специальных справочных таблицах. [7]
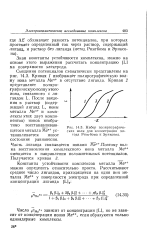 |
Набор полярографических волн для иллюстрации метода Рингбома и Эриксона. [8] |
Поэтому волна восстановления комплексного иона металла Мел смещается в направлении положительных потенциалов. [9]
Если при диссоциации комплексных ионов металла в растворе происходит заметное изменение концентрации исходного комплекса либо образующихся продуктов, то при наличии электродов, обратимых по отношению к тому или иному участнику реакции, либо к частицам, находящимся в равновесий с ними, можно определять скорость диссоциации комплекса потенциометрическим методом. [10]
Измерения порядка реакций разряда комплексных ионов металлов оказались особенно полезными при разрешении давно возникшего вопроса, предшествует ли переносу заряда диссоциация. Механизм разряда таких ионов обсуждался в течение многих лет и был наконец расшифрован. [11]
В выражение потенциала полуволны комплексного иона металла не входит концентрация ионов этого металла, и, следовательно, е z не зависит от концентрации деполяризатора. [12]
Образующиеся при протекании реакции акватации комплексные ионы металлов часто обладают свойствами слабых кислот, что связано с относительно легким отщеплением ионов водорода от молекул воды, находящихся во внутренней координационной сфере комплекса. В подобных случаях скорость реакции акватации может быть определена путем измерений во времени рН исследуемого раствора. Измерения рН обычно проводят со стеклянным электродом в нейтральных или близких к нейтральным средах, не содержащих буферных добавок. [13]
Кинетические ограничения полярографического тока при разряде комплексных ионов металлов были впервые обнаружены И. [14]
Кинетические токи наблюдаются при восстановлении некоторых комплексных ионов металлов. Предшествующая химическая реакция в подобных случаях заключается в отщеплении одной или нескольких частиц лиганда от преимущественно присутствующих в растворе комплексов. Подробнее этот вопрос рассматривается в гл. Здесь же мы рассмотрим лишь основные свойства кинетических предельных токов, которые позволяют отличать их от диффузионных предельных токов. [15]
Страницы: 1 2 3 4