Комплексный ион - металл
Cтраница 3
Однако уравнение потенциала полуволны включает величину константы диссоциации комплексного иона и потому зависит от логарифма константы диссоциации комплексного иона металла. [31]
Ниже будут рассмотрены наиболее распространенные в аналитическом направлении виды подобной полярографической каталиметрии: 1) каталитический ток простых и комплексных ионов металлов, 2) каталитический ток окислителей, 3) каталитический ток ионов водорода. [32]
В комплексных электролитах анодный процесс может протекать в результате ионизации металла с образованием простейших комплексных ионов, а также перезарядки уже имеющихся комплексных ионов металла до высшей формы окисления центрального иона. [33]
Абе и Вада [1] в своей работе приводят спектры поглощения и радиусы Стокса ( вычислены по результатам кондуктометрических измерений) сольватированных комплексных ионов металлов первого переходного ряда в гексаметилфосфортриамиде. Они нашли, что радиусы Стокса этих комплексных ионов весьма чувствительны к изменениям конфигурации, поскольку диаметр молекулы указанного растворителя велик по сравнению с кристаллографическим диаметром центральных ионов металла. Найдено, что гексаметилфосфортриамидом солъватируются ионы Mn ( II), Fe ( II), Co ( II) и Си ( II), в то время как для Ni ( II) устанавливается равновесие для октаэдрических, плоскоквадратных и тетраэдрических сольватированных частиц. По-видимому, Zn ( II) дает октаэдрический комплексный ион, сольватированный гексаметилфосфортриамидом. [34]
Следует отметить, что полученные нами данные не согласуются с выводами Измайлова [295] о корреляции между величинами энергии активации и константами нестойкости комплексных ионов металлов, а также о взаимосвязи между величиной этой энергии при диффузионном контроле процесса и валентностью центрального атома в комплексе. [35]
Одним из методов тонкой очистки неорганических веществ является комплексоадсорбдионный метод, в котором в качестве сорбентов используются активные угли, поглощающие из растворов солей органические вещества и комплексные ионы металлов. Активный уголь практически не набухает в воде и имеет достаточно жесткую структуру, стоек к растворам минеральных и органических кислот, солей, некоторых оснований и обладает способностью выдерживать в определенных условиях достаточно жесткие температурные воздействия. [36]
Кс - константа диссоциации комплексного иона; Сх - концентрация комплексообразующего вещества X на поверхности электрода; kc и k & - пропорциональны квадратным корням из коэффициентов диффузии комплексных ионов металлов и металла в амальгаме; aHg - активность ртути у поверхности капающего электрода. [37]
Анодный процесс в комплексном электролите может протекать за счет окисления атомов металла, в результате которого образуются комплексные ионы, или за счет окисления уже присутствующих в растворе комплексных ионов металла до более высокого окислительного состояния центрального иона. Анодные процессы окисления лигандов, например галогенид-ионов, которые также могут протекать в комплексных электролитах, мы рассматривать не будем. [38]
Подводя итоги, можно сказать, что если восстановление иона металла происходит из комплексного иона, то потенциал полуволны так же, как и в случае восстановления простых ионов, не зависит от концентрации комплексных ионов металла в растворе. [39]
Здесь рассмотрены такие три примера применения этого метода, в случае которых не требуется детального анализа влияния заполнения электрода сильно адсорбирующимися молекулами исходных или конечных продуктов ( гл, X): редокс-системы, состоящие из растворимых частиц, разряд комплексных ионов металлов и разряд иона водорода на ртути. [40]
Электровосстановлению на ртутном капающем электроде могут подвергаться не только простые, но также и комплексные ионы металлов. Потенциалы полуволн комплексных ионов металлов смещаются к более отрицательным значениям относительно потенциалов простых ионов. Величина этого смещения является функцией концентрации лигандов, а также устойчивости образующегося комплекса, что позволяет пользоваться полярографическим методом как для определения констант нестойкости комплексов, так и для выяснения их состава. Вполне естественно, что это возможно только при условии, что на сдвиг потенциалов полуволн не влияют другие факторы - необратимость диссоциации комплексов, необратимость их восстановления и др. Правда, случаи необратимого восстановления комплексов встречались до последнего времени в литературе не так часто. [41]
Цианидные растворы применяют при электропокрытии золотом, серебром, цинком, кадмием и другими металлами. Концентрация jie - комплексных ионов металла в этих растворах очень мала, что способствует получению однородных тонкозернистых покрытий. Другие анионы, образующие комплексы ( тартрат, цитрат, хлорид, гидроксил), также применяют в растворах, используемых при получении покрытий. [42]
Как видно отсюда, процессы комплексообразования указанных элементов в НС1 протекают ступенчато. Соотношение между отдельными формами комплексных ионов металла зависит от концентрации комплексообразующего агента. То же самое можно сказать и относительно комплексообразования трехвалентных трансурановых элементов, в том числе и Am ( III), в растворах других неорганических кислот. [43]
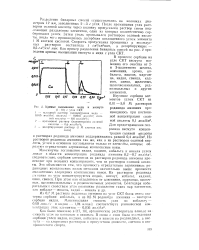 |
Кривые вымывания меди ( 1. 10 с угля СКТ. [44] |
Максимумы поглощения индия, кадмия, кобальта и никеля углем лежат в области концентрации роданида аммония 0 2 - 0 7 мол / дм, следовательно, сорбция элементов из растворов роданида аммония происходит при меньших концентрациях, чем из растворов соляной кислоты. Это объясняется тем, что прочность отрицательно заряженных ро-данидных комплексных ионов металлов значительно выше прочности аналогичных хлоридных комплексных ионов. Из растворов роданида аммония на угле концентрируются индий, висмут, кобальт, кадмий, цинк, свинец. При этом они отделяются от алюминия, марганца, щелочных, щелочноземельных и редкоземельных элементов. [45]
Страницы: 1 2 3 4