Комплексный ион - металл
Cтраница 2
 |
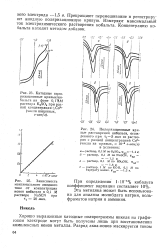
Поляризационные кривые при замедленной химической реакции диссоциации преобладающего комплекса. [16] |
При электроосаждении металлов из электролитов, содержащих комплексные ионы металла, возможен разряд различных сортов частиц. В простейших случаях это могут быть простые незакомплексованные ионы металла, комплексные ионы, преобладающие в растворе, или комплексные ионы, образующиеся в результате химической реакции диссоциации преобладающих комплексов. В последнем случае стадии разряда предшествует стадия диссоциации преобладающего комплекса. Такая предшествующая разряду химическая реакция может быть быстрой по сравнению со стадией разряда либо может лимитировать скорость процесса в целом. [17]
В присутствии соответствующих комплексообразовате-лей на анодных участках образуются комплексные ионы металла. Уменьшение концентрации простых ионов металла у анода ведет к увеличению скорости анодного процесса. В случаях, когда анодный процесс бывает заторможенным, появление в растворе мощного комплексообразователя сопровождается существенным увеличением скорости - коррозии. Известно, например, что при одновременном присутствии в растворе растворенного кислорода и аммиака последний является анодным ускорителем для меди и медных сплавов, поскольку ионы меди связываются аммиаком в медно-аммиачные комплексы. Даже такие коррозионно-стойкие металлы, как серебро и золото, начинают растворяться, если в растворе присутствуют цианиды CN -, являющиеся для Ag и Аи активными комплексообразователями. [18]
 |
Потенциалы полуволн восстановления комплексных соединений никеля. [19] |
Следует иметь в виду, что потенциалы полуволн восстановления комплексных ионов металлов отличаются от потенциалов полуволн простых ионов и зависят от констант устойчивости комплекса. [20]
В литературе описано несколько потенциометрических методов изучения скоростей реакции акватации комплексных ионов металлов в водных растворах электролитов. [21]
Отсутствие прямой связи между константой равновесия и величиной перенапряжения при восстановлении комплексных ионов металла [37, 38] дает основание предполагать, что и в случае аква-комплекса прочность его также не должна оказывать существенного влияния на протекание электродного процесса. [22]
Повышение значения рН в большинстве случаев способствует образованию более сложных по составу комплексных ионов металла, как, например, в щелочных и щелочно-цианистых, пирофос-фатных, аминокомплексных и других электролитах. При этом равновесный потенциал катода смещается в сторону более электроотрицательных значений, во многих случаях повышается также катодная поляризация и уменьшается размер кристаллов в осадках. [23]
Существует множество подобных автокаталитических процессов, протекание которых зависит от легкости окисления субстрата комплексным ионом металла и возможности регенерации окисленной формы последнего кислородом воздуха. Еще одним примером реакций этого типа является катализ ионами Си ( II) авто-окисления аскорбиновой кислоты [32] ( гл. [24]
Электровосстановлению на ртутном капающем электроде могут подвергаться не только простые, но также и комплексные ионы металлов. Потенциалы полуволн комплексных ионов металлов смещаются к более отрицательным значениям относительно потенциалов простых ионов. Величина этого смещения является функцией концентрации лигандов, а также устойчивости образующегося комплекса, что позволяет пользоваться полярографическим методом как для определения констант нестойкости комплексов, так и для выяснения их состава. Вполне естественно, что это возможно только при условии, что на сдвиг потенциалов полуволн не влияют другие факторы - необратимость диссоциации комплексов, необратимость их восстановления и др. Правда, случаи необратимого восстановления комплексов встречались до последнего времени в литературе не так часто. [25]
Хорошо выраженные катодные полярограммы никеля на графитовом электроде могут быть получены лишь при восстановлении комплексных ионов металла. [27]
Как известно, электроосаждение металлов проводят из растворов, содержащих как простые, так и комплексные ионы металлов. На присутствие в растворе комплексных ионов указывает сдвиг равновесного потенциала в отрицательную сторону по сравнению с раствором, содержащим простые ионы. [28]
Потенциал полуволны иона металла, восстанавливающегося из комплексного соединения, зависит от логарифма константы диссоциации комплексного иона металла. [29]
Способы получения металлических покрытий путем химического восстановления в растворах основаны на реакции взаимодействия простых или комплексных ионов металла с растворенным восстановителем, в результате которой на каталитически активную поверхность оседает металлический слой. Для ссаждения необходимо, чтобы растворенный восстановитель был достаточно сильным и активным, а образовавшийся металл действовал на реакцию восстановления как катализатор. Это обеспечивает получение компактного покрытия значительной ( десятки микрометров) толщины. [30]
Страницы: 1 2 3 4