Комплексный ион - металл
Cтраница 4
В этом уравнении все величины могут быть найдены экспериментально. KsjKc определяется из отношения наблюдаемых диффузионных токов простых и комплексных ионов металлов при одной и той же концентрации и всех прочих равных условиях. [46]
В растворах комплексных солей металлов концентрация водородных ионов влияет как на состав комплексных ионов, так и на устойчивость комплексных соединений, что в свою очередь отражается на катодной поляризации и структуре осадков. Повышение значений рН в большинстве случаев способствует образованию более сложных по составу комплексных ионов металла, как, например, в щелочных и щелочно-цианистых, пирофосфатных, ами-нокомплексных и других электролитах. При этом равновесный потенциал катода смещается в сторону электроотрицательных значений, во многих случаях повышается также катодная поляризация и уменьшается размер кристаллов в осадках. [47]
В работах [230-234], используя переменнотоковую полярографию, по каталитическим волнам восстановления простых и комплексных ионов металлов успешно определяли металлы. Поскольку в присутствии лиганда-катализатора электрохимическая стадия переноса электронов значительно ускоряется, давая близкую к обратимой или полностью обратимую волну, то переменнотоковая полярография позволяет заметно понизить предел определения металлов. Таким путем были разработаны [230-234] методики высокочувствительного определения кобальта ( II), никеля ( II) и европия ( III) с применением в качестве лигандов-катализаторов гетероциклических аминов. Методики также отличаются достаточно высокой селективностью. [48]
Сорбируемость ионов второй группы - меди, бериллия, кобальта, никеля, олова ( II), алюминия, висмута, индия, церия ( III), титана, циркония и ванадия ( V) - проходит через максимум и достигает небольшой величины. Увеличение сорбируемости элементов этой группы с ростом концентрации азотной кислоты объясняется увеличением концентрации комплексных ионов металлов, способных сорбироваться анионитами. Уменьшение; же их сорбируемости связано с конкурирующим влиянием нитратных групп азотной кислоты. [49]
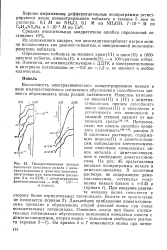
Возможность электрохимического концентрирования никеля в виде малорастворимого соединения обусловлена способностью элемента образовывать ионы разной валентности. В щелочных растворах, содержащих никель ( II) и диметилглиок-сим, наблюдается электрохимическое окисление комплексных ионов металла с диметилглиокси-мом и свободного диметилглиок-сима. На рис. 45 представлены анодные полярограммы никеля и диметилглиоксима. [51]
Концентрационную поляризацию вызывают побочные газовыде-ляющие процессы у электродов при диссоциации воды. Химическая поляризация является результатом ограниченной скорости протекания химических реакций в приэлектродном слое электролита вследствие замедленной диссоциации комплексных ионов металла. Химическую поляризацию можно устранить добавлением комплек-сообразователсй, которые увеличивают электроотрицательность потенциала. [52]
Рассмотрим теперь несколько примеров того, как скорости реакций и их механизмы влияют на поведение соединений. Большинство ионов металлов даже в закомплексованном виде очень быстро реагируют с льюисовыми основаниями, и только небольшое число некоторых комплексных ионов металлов реагируют медленно. Комплексы металлов считаются кинетически лабильными, если при комнатной температуре они успевают полностью прореагировать за время, необходимое для смешивания 0 1 М растворов реагентов. Если же реакции комплексов при комнатной температуре протекают достаточно медленно, чтобы их скорость можно было измерить традиционными методами, эти комплексы определяют как кинетически инертные. Важно не путать кинетическую устойчивость, описываемую терминами инертный и лабильный, с устойчивостью термодинамической. Инертный ион Co ( NH3) e 1, термодинамически неустойчивый в кислом растворе, не реагирует сколько-нибудь заметно с кислотой в течение нескольких дней. В лабильном ионе Ni ( CN) 4 -, который термодинамически весьма устойчив, обмен цианид-ионов ( измеряемый с помощью меченых цианид-ионов) протекает настолько быстро, что скорость этого процесса невозможно измерить обычными методами. [53]
Страницы: 1 2 3 4