Титруемый ион
Cтраница 1
Титруемый ион и титрант могут быть поляро-графически неактивны. [1]
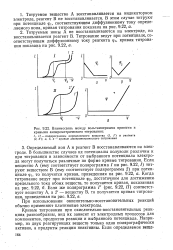 |
Взаимосвязь между вольтамперными кривыми и кривыми амперометрического титровдния. [2] |
Титруемые ионы А не восстанавливаются на электроде, но восстанавливается реагент В. [3]
Титруемый ион Fe представляет собой компонент обратимой редокс пары, а ион титранта - С Г 2 7 - - необратимой. [4]
Если титруемый ион образует с ионом серебра соль, более растворимую, чем AgCl, то условия для применения хромата Б качестве индикатора становятся менее благоприятными. [5]
 |
Принцип действия металлоиндикатора. [6] |
Если титруемые ионы металла в условиях, при которых проводят титрование, практически не образуют гидроксокомплексы, левая ветвь кривых титрования от рН не зависит. [7]
При титровании концентрация титруемых ионов постепенно уменьшается, а концентрация реагирующих с ними ионов рабочего раствора постепенно увеличивается. [8]
Наиболее резко меняется концентрация титруемых ионов вблизи точки эквивалентности. [9]
На окислительный потенциал влияют концентрации титруемых ионов и посторонних веществ, изменяющих ионную силу раствора, а следовательно, и активности реагирующих ионов, учитываемые формулой Нернста. Например, при малой концентрации бихромат калия в сернокислой среде не окисляет хлорид-иона до свободного хлора. Однако концентрированные растворы бихромата калия в присутствии концентрированной серной кислоты выделяют свободный хлор из раствора, содержащего хлорид-ион. Взаимодействие между окислителем и восстановителем происходит до тех пор, пока между ними существует разница окислительных потенциалов, которую можно вычислить по формуле Нернста. [10]
После достижения точки эквивалентности, когда титруемые ионы галогенов полностью прореагируют с ионами ртути ( II), в титруемом растворе появляются избыточные свободные Hg - noHbi, которые обнаруживают при помощи соответствующего индикатора, образующего с Н § - ионами характерные соединения. [11]
После достижения точки эквивалентности, когда титруемые ионы галогенов полностью прореагируют с ионами ртути ( II), в титруемом растворе появляются избыточные свободные Hg - HOHbi, которые обнаруживают при помощи соответствующего индикатора, образующего с Hg - HOHaMH характерные соединения. [12]
Кривые титрования, показывающие изменение концентрации титруемых ионов, в зависимости от количества прибавленного рабочего раствора, аналогичны Кривым титрования по другим реакциям. Если реакция идет в несколько ступеней, соответственно несколько ступеней имеет и кривая титрования. [13]
Вообще ход титрования зависит от изменения концентрации титруемого иона и в конечном счете зависит от свойств титруемого вещества. Различие между индикаторным и потенциометрическим титрованием представляет только различие в методе оценки изменения концентрации титруемого иона вблизи точки эквивалентности. [14]
Если неизотопный индикатор способен изоморфно соосаждаться с титруемым ионом, то желательно введение возможно меньшего количества индикатора, но с достаточно большой удельной активностью. Применение неизотопных изоморфных индикаторов целе сообразно, если определяемый элемент не имеет подходящих радиоактивных изотопов. [15]
Страницы: 1 2 3 4 5