Титруемый ион
Cтраница 3
Одноцветные индикаторы представляют собой бесцветные комплексообразующие реагенты, которые дают окрашенные комплексы с титруемым ионом металла. [31]
Ионы других металлов, присутствующие в растворе примерно в такой же концентрации, как титруемые ионы железа ( III), практически не мешают, если в комплексонаты превращаются не более 0 1 % этих ионов. Из рис. 45 видно, что, если ионы железа ( III) титруют при рН 2, реагент по отношению к ионам щелочноземельных металлов ( Mg2, Ca2, Ва2) замаскирован. [32]
Ионы других металлов, присутствующие в растворе примерно в такой же концентрации, как титруемые ионы железа ( III), практически не мешают, если в комплексонаты превращается не более 0 1 % этих ионов. Из рис. 50 видно, что, если ионы железа ( III) титруют при рН 2, реагент по отношению к ионам щелочноземельных металлов ( Mg2, Ca2, Ва2) замаскирован. [33]
 |
Прибор для внутреннего электролиза. [34] |
Потенциометрический метод анализа основан на измерении электродного потенциала и изменении величины его от концентрации титруемого иона. [35]
Из этого уравнения следует, что чем выше рН раствора, тем меньше концентрация титруемых ионов в свободном состоянии в точке эквивалентности. [36]
При хелатометрическом титровании точку эквивалентности устанавливают с помощью металлохромных индикаторов, которые образуют с титруемыми ионами растворимые, окрашенные комплексные соединения, менее устойчивые, чем комплексные соединения определяемых ионов с ЭДТА. При добавлении к таким комплексам Ме-индикатор ЭДТА образуется более прочный комплекс металла с ЭДТА, а индикатор высвобождается и придает раствору соответствующую окраску. [37]
 |
Прибор для внутреннего электролиза. [38] |
Потенциометр ический метод анализа основан на измерении электродного потенциала и изменении величины его от концентрации титруемого иона. [39]
Из уравнения видно, что относительная ошибка тем меньше, чем выше устойчивость комплекса и общая концентрация титруемого иона металла. Уравнение (5.18) не учитывает ионы металла, еще связанные с индикатором в точке эквивалентности, однако это несущественно, если См значительно превышает аналитическую концентрацию индикатора. [40]
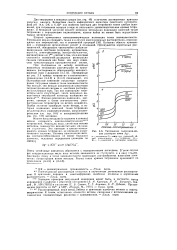 |
Титрование галогенид-ио-нов раствором ионов Ag. [41] |
Приведенные на рис. 3.6 кривые титрования в соответствии с уравнениями (3.4.5) и (3.4.4) показывают, что скачкообразное изменение показателя концентрации титруемых ионов в точке эквивалентности тем меньше, чем меньше концентрация реактивов титриметрической системы и чем более растворима осаждающая соль. [42]
Однако даже введение поправочных коэффициентов позволяет снизить погрешность анализа до 0 2 % лишь в том случае, когда концентрация титруемого иона в 50 раз превосходит значение равновесной концентрации этого же иона, найденное из произведения растворимости. [43]
Следовательно, при потенциометрическом титровании по методу осаждения потенциал определяют по формуле Нернста, подставляя в нее величину остаточной концентрации титруемого иона. Потенциал в точке эквивалентности определяют по концентрации насыщенного раствора, находящегося над осадком, которую вычисляют по произведению растворимости. Потенциал за точкой эквивалентности определяют, подставляя в формулу Нернста величину концентрации определяемого иона в присутствии избытка осадктеля. Эту концентрацию также определяют по произведению растворимости осадка. [44]
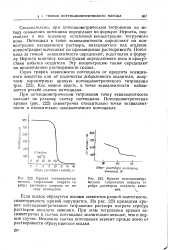 |
Кривая потенциометрического титрования нитрата серебра раствором хлорида по методу осаждения.| Кривая потенциометрн ческого титрования нитрата серебра раствором оксалата аммония. V. [45] |
Страницы: 1 2 3 4 5