Титруемый ион
Cтраница 4
Следовательно, при потенциометрическом титровании по методу осаждения потенциал определяют по формуле Нернста, подставляя в нее величину остаточной концентрации титруемого иона. Потенциал в точке эквивалентности определяют по концентрации насыщенного раствора, находящегося над осадком; концентрацию вычисляют по произведению растворимости. Потенциал за точкой экивалентности определяют, подставляя в формулу Нернста величину концентрации определяемого иона в присутствии избытка осадителя. Эту концентрацию также определяют по произведению растворимости осадка. [46]
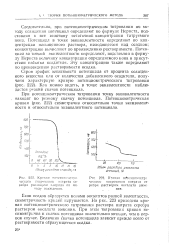 |
Ктшпзя п (. геш. иометр.. ческою титрования нитрата серебра раствором оксалата аммония. [47] |
Следовательно, при потенциометрическом титровании по методу осаждения потенциал определяют по формуле Hep иста, подставляя в нее величину остаточной концентрации титруемого иона. Потенциал в точке эквивалентности определяют по концентрации насыщенного раствора, находящегося над осадком; концентрацию вычисляют по произведению растворимости. Потенциал за точкой экивалентности определяют, подставляя в формулу Нернста величину концентрации определяемого иона в присутствии избытка осадителя. Эту концентрацию также определяют по произведению растворимости осадка. [48]
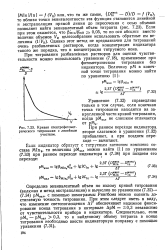 |
Кривая спектрофотомет. [49] |
Однако этот метод не предназначен для титрований очень разбавленных растворов, когда концентрация индикатора такого же порядка, что и концентрация титруемого иона. [50]
Положительный эффект достигается за счет того, что для расчета концентрации анализируемого иона используются результаты титрования, полученные в условиях значительного избытка титруемого иона, превосходящего равновесную концентрацию этого иона, вычисленную из значения произведения растворимости осадка или из значения константы комплексообразования образующегося при титровании соединения. При этом зависимость потенциала электрода от концентрации титруемого иона измеряется в оптимальном интервале, где флуктуация крутизны электродной функции минимальна. Высокие значения остаточной концентрации титруемого иона делают пренебрежимо малым вклад в его суммарную концентрацию растворимости осадка и образования комплексных соединений, стехиометрия которых отличается от стехиометрии основного продукта реакции титрования. [51]
С одной стороны, разбавление титрованного раствора реактива выгодно, так как 1 мл такого разбавленного раствора будет соответствовать тем меньшему количеству титруемого иона, чем сильнее разбавление, но, с другой стороны, чем разбавлен-нее раствор, тем при титровании труднее четко уловить момент конца титрования. Для повышения четкости перехода окраски индикатора полезно иметь как можно меньший объем раствора, в котором производится титрование. Вопрос об ошибках микротитрования обсуждается в конце этого раздела. [52]
 |
Схема автоматического титратора. [53] |
Электрическая схема через систему реле выключает электродвигатель в тот момент, когда потенциал индикаторного электрода достигает заранее установленной экспериментатором величины, характерной для концентрации титруемых ионов в точке эквивалентности. [54]
Таким образом, ПР последовательно образующихся при титровании осадков должны отличаться друг от друга не менее, чем на три порядка при условии равенства начальных концентраций титруемых ионов. [55]
 |
Типичная кривая pax изменение потенциала А. доста-титро - точно велико. Для слабой кислоты и сильного основания ( или наоборот можно удовлетворительно определить. [56] |
Точность измерения конечной точки титрования определяется степенью изгиба кривой, которая зависит от величины константы диссоциации ( или произведения растворимости в случае осаждения) и концентрации титруемых ионов. [57]
Индикаторный электрод выбирают в зависимости от типа реакций, лежащих в основе титрования, но во всех случаях потенциал электрода должен устанавливаться практически мгновенно в соответствии с концентрацией титруемых ионов и не зависеть от присутствия других ионов. [58]
Из этих равенств вытекает, что ПР последовательно образующихся при титровании с заданной точностью бинарных осадков должны отличаться друг от друга л / в 10ОО раз при условии равенства начальных концентраций титруемых ионов. [59]
Поэтому после точки эквивалентности сила тока, соответствующая восстановлению или окислению на электроде иона титранта, может быть значительной, и перегиб кривой титрования в эквивалентной точке будет резким, несмотря на малую концентрацию титруемого иона. [60]
Страницы: 1 2 3 4 5