Галогеналкан
Cтраница 3
Повышенная относительная плотность галогеналканов объясняется присутствием атома галогена; его влияние тем больше, чем меньше углеводородный радикал. [31]
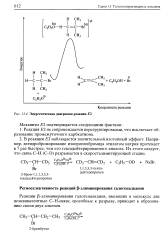 |
Энергетическая диаграмма реакции Е2. [32] |
Реакции ( 3-элиминирования галогеналканов, имеющих в молекуле две неэквивалентные С - Н - связи, способные к разрыву, приводят к образованию смеси двух алкенов. [33]
Взаимодействие пиридина с галогеналканами приводит к образованию солей алкилпиридиния. [34]
Реакция феноксид-аниона с галогеналканом известна под названием синтеза Вильямсона. [35]
Взаимодействием анилина с галогеналканами получают вторичные и третичные алкилароматические амины. [36]
Подводя итог рассмотрению конформации галогеналканов, подчеркнем еще раз главный вывод: между заместителями существуют не только силы отталкивания, не только пространственные препятствия, но и силы притяжения, обусловливающие создание соответствующих конформации. [37]
В некоторых случаях восстановление галогеналканов действием цинка в водной минеральной или уксусной кислоте является удобным лабораторным способом получения алканов. [38]
Ниже даны примеры названий галогеналканов по номенклатуре ИЮПАК. [39]
При этом реакционная способность галогеналканов падает в ряду: R - I R - Br R - Cl. Реакция Вюрца пригодна для получения прежде всего высших алканов с четным числом атомов углерода. [40]
Рассмотренные выше реакции получения галогеналканов из спиртов протекают значительно более гладко, если спирты предварительно обрабатывают и-толуолсульфонилхлоридом в присутствии пиридина. [41]
Спирты в отличие от галогеналканов не могут подвергаться элиминированию по чистому механизму Е2, так как для реакций Е2 требуется сравнительно сильное основание, способное отщеплять протон от Co-атома. Сильное основание и кислая среда несовместимы: сильное основание гораздо быстрее, чем спирт, протонируется минеральной кислотой или спиртом. [42]
Химики активно ищут замену галогеналканам ( хлороформ, ди - и тетра-хлорэтаны), в огромных объемах применяемым в качестве растворителей в различных отраслях промышленности. Одной из перспективных находок считается этиловый эфир молочной кислоты - этиллактат, обладающий высокой растворяющей способностью по отношению ко многим продуктам. В противоположность галогеналканам, основу производства которых составляют продукты переработки нефти, сырьем для получения этиллак-тата являются сельскохозяйственные культуры - кукуруза и сахарная свекла. Это обстоятельство обусловливает его хорошую биоразлагаемость и как следствие безвредность для окружающей среды. [43]
При взаимодействии алкоголятов с галогеналканами образуются простые эфиры. Простыми эфирами называются производные спиртов, в которых атом водорода гидроксильной группы заменен на углеводородный радикал. Реакция протекает по механизму нуклеофильного замещения. В качестве нуклеофила выступает алко-голят-ион, нуклеофильность которого выше, чем нейтральной молекулы спирта. [44]
Эту реакцию также называют аммонолизом галогеналканов. Образующийся в ходе реакции галогеноводород взаимодействует с амином, давая аммониевую соль. В приведенной ниже реакции нуклеофилом служит нейтральная молекула аммиака, в которой атом азота имеет неподеленную пару электронов. [45]
Страницы: 1 2 3 4