Галогениды - щелочной металл
Cтраница 1
Галогениды щелочных металлов гораздо лучше растворяются в трихлориде сурьмы, чем в трихлориде мышьяка. Коэффициенты Вант-Гоффа для некоторых одно-одновалентных электролитов, определенные из криоскопических данных, при бесконечном разбавлении стремятся к предельному значению, равному двум. [1]
Галогениды щелочных металлов являются модельными объектами для физики высоких давлений. Эти материалы достаточно подробно исследованы. Свойства этих соединений при высоких давлениях практически не изучены. [3]
Галогениды щелочных металлов во многих отношениях сходны с гало-генидами серебра, но в них наблюдается разупорядочение по Шоттки, а не по Френкелю. [4]
Галогениды щелочных металлов занимают в теории структур особое место. Применительно к ним было проведено громадное количество расчетных и экспериментальных работ. [5]
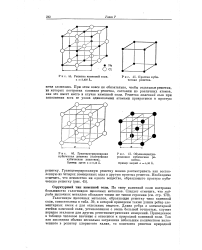 |
Решетка каменной соли, а 5 628 А.| Простая кубическая решетка. [6] |
Галогениды щелочных металлов, образующие решетку типа каменной соли, сопоставлены в табл. 39, в которой приведены также длины ребер элементарных ячеек а для отдельных веществ. Длина ребра а элементарной ячейки каменной соли, установленная с очень большой точностью, служит нередко эталоном для других рентгенометрических измерений. Приведенное в таблице числовое значение а относится к природной каменной соли. [7]
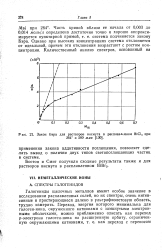 |
Закон Бэра для растворов висмута в расплавленном В1С13 при. [8] |
Галогениды щелочных металлов имеют особое значение в исследовании расплавленных солей, но их спектры, очень интенсивные и простирающиеся далеко в ультрафиолетовую область, трудно измерить. [9]
Галогениды щелочных металлов ( за исключением, может быть, лития), щелочноземельных металлов ( кроме бериллия) и большинства лантанидов и нескольких галогенидов актинидов можно считать чисто ионными галогенидами. По мере увеличения отношения заряд / радиус, однако, ковалентность возрастает. KCI - чисто ионное соединение, тогда как TiCl4 фактически ковалентное. Нечто подобное имеет место и для металлов с переменной степенью окисления; низшие галогениды в большей мере являются ионными, в то время как высшие галогениды - ковалентные соединения. В качестве примеров можно привести РЬС12 и РЬС14, а также UF4, который является ионным соединением, тогда как UFe - газообразное ковалентное соединение. [10]
Галогениды щелочных металлов были исследованы в газе микроволновым методом и методом молекулярных пучков. [11]
 |
Физические свойства оксигалогенидов органических кислот. [12] |
Галогениды щелочных металлов практически не сольватируются и, следовательно, очень мало растворимы в жидком нитрозилхлориде. [13]
Галогениды щелочных металлов и тетраалкиламмония образуют стабильные комплексы со многими алюминийалкилами. [14]
Галогениды щелочных металлов в процессах диффузионного насыщения используют довольно широко. Реакции, лежащие в основе активирующего действия этих добавок, пока окончательно не выяснены. [15]
Страницы: 1 2 3 4