Галогениды - щелочной металл
Cтраница 3
Несмотря на указанные сложности, галогениды щелочных металлов относятся к системам, для которых выполняется неравенство Ks Ki - В кристалле, который находится в равновесии с паром металла, концентрация избыточных атомов металла пропорциональна парциальному давлению рм. Это указывает на образование одиночных неионизированных вакансий галогена ( наблюдаемых как F-центры) [25 - 26] при вхождении избытка металла в твердую фазу ( рис. XIII. Нейтральность дефектов связана с большой энергией ионизации. Фактически наблюдаемое расстояние F-уровня ( или Vx-уровня) до зоны проводимости составляет приблизительно 1 5 эв. В то же время отсутствие ассоциатов не вызывает удивления, поскольку связано с незначительной энергией ассоциации, которая ожидается для вакансий галогена. Следовало бы ожидать, что при введении лишних атомов галогена концентрация дефектов окажется пропорциональной р, если образуются однократно ионизированные вакансии металла, и р ] Ц, если возникают нейтральные одиночные дефекты. [31]
Наиболее эффективными катализаторами процесса являются галогениды щелочных металлов и четвертичных аммониевых оснований. [32]
Классическими представителями ионных кристаллов являются галогениды щелочных металлов. Катионы М и анионы Х - расположены упорядоченно в кубической решетке: каждый анион непосредственно окружен находящимися на расстоянии г от него 6 катионами, и наоборот. [33]
 |
Схема расположения частиц на поверхности кристалла. [34] |
Сомораи [99] предполагает, что галогениды щелочных металлов имеют низкую поверхностную диффузию. Отсутствие заметной поверхностной диффузии препятствует достижению устойчивой концентрации выступов и узлов. Повышение плотности дислокаций на поверхности напряженного кристалла, по-видимому, увеличивает концентрацию участков ( узлов или выступов), с которых происходит испарение. Поэтому с увеличением плотности дислокаций у рассматриваемых веществ повышается скорость сублимации. Однако большинство твердых веществ проявляют постоянную скорость испарения ( после короткого периода индукции) при данной температуре, не зависящую от плотности дислокаций. [35]
Классическими представителями ионных кристаллов являются галогениды щелочных металлов. Катионы М и анионы X-расположены упорядоченно в кубической решетке: каждый анион непосредственно окружен находящимися на расстоянии г от него 6 катионами, и наоборот. [36]
 |
Схема расположения частиц на поверхности кристалла. [37] |
Сомораи [99] предполагает, что галогениды щелочных металлов имеют низкую поверхностную диффузию. Отсутствие заметной поверхностной диффузии препятствует достижению устойчивой концентрации выступов и узлов. Повышение плотности дислокаций на поверхности напряженного кристалла, по-видимому, увеличивает концентрацию участков ( узлов или выступов), с которых происходит испарение. Поэтому с увеличением плотности дислокаций у рассматриваемых веществ повышается скорость сублимации. Однако большинство твердых веществ проявляют постоянную скорость испарения ( после короткого периода индукции) при данной температуре, не зависящую от плотности дислокаций. [38]
Для простых ионных веществ, как галогениды щелочных металлов, имеется очень небольшой выбор возможных структур. Различные факторы, влияющие на устойчивость кристаллов, лротиводействуют друг другу. Окончательный выбор между решеткой хлористого натрия и хлористого цезия не является четко выраженным результатом влияния какого-либо одного фактора. Для сложных веществ, как слюда КА1з51зОю ( ОН) 2 или цуниит AliaSisC o ( ОН) 18С1, можно предложить очень много приемлемых структур, мало отличающихся по характеру и стабильности. Можно ожидать, что наиболее устойчивая из возможных структур, которая и существует в действительности, отражает влияние различных факторов, играющих существенную роль при определении строения ионных кристаллов. Оказалось, что можно сформулировать ряд правил относительно устойчивости сложных ионных кристаллов. Мы рассмотрим эти правила в следующих разделах. [39]
В бромиде алюминия ( Ш) галогениды щелочных металлов обычно растворяются с образованием тетрабромоалюминатов; они также хорошо растворимы в расплавленном бромиде ртути ( П), из растворов которой могут быть выделены трибромоиеркураты. [40]
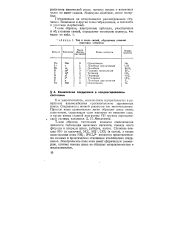 |
Тип и число связей, образуемых атомами некоторых элементов. [41] |
Таким образом, типичными ионными соединениями являются галогениды щелочных металлов, прежде всего фториды и хлориды цезия, рубидия, калия. Сложные анионы ОН - ( в щелочах), NCXr, SO, ClQr ( в солях), а также комплексные ионы ЫЩ, ( PtCle ] a - являются представителями важных в практическом отношении комплексных соединений. Электрическое поле иона имеет сферическую симметрию, поэтому ионная связь не обладает направленностью и насыщаемостью. [42]
Таким образом, типичными ионными соединениями являются галогениды щелочных металлов, прежде всего фториды и хлориды цезия, рубидия, калия. [43]
Как было показано в предыдущем разделе, галогениды щелочных металлов - наиболее эффективные ингибиторы цепных процессов воспламенения углеводородов. [44]
В ионных кристаллах, простейшими представителями которых являются галогениды щелочных металлов ( например, хлористый натрий NaCl ( фиг. [45]
Страницы: 1 2 3 4